Síntesis de péptidos
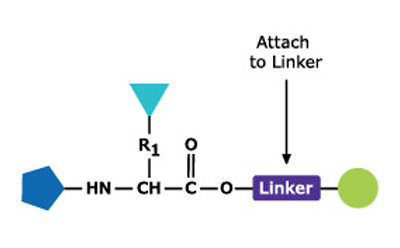
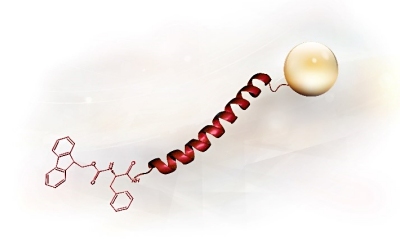
Un péptido está formado por dos o más aminoácidos unidos por un enlace amida, que forman una cadena de aminoácidos que suele tener una longitud de entre 2 y 70 aminoácidos. Los péptidos se distinguen de las proteínas en que no necesitan plegarse para tener actividad biológica. Los péptidos se producen de forma endógena como hormonas peptídicas, tales como la angiotensina, la LHRH y la encefalina, y como toxinas en plantas y animales. Los péptidos son de gran interés como compuestos principales para el descubrimiento de fármacos y como fármacos por derecho propio. También tienen aplicaciones en vacunas, biomateriales y sondas histológicas, y se utilizan en grandes cantidades como antígenos para generar anticuerpos.
Los péptidos se sintetizan químicamente en solución o en fase sólida. El proceso implica la formación dirigida y selectiva de un enlace amida entre un aminoácido N-protegido y un aminoácido que lleva un grupo amino libre y un ácido carboxílico protegido. En la síntesis en fase sólida, el grupo protector del carboxilo se une a un soporte polimérico. Tras la formación del enlace, se elimina el grupo protector amino del dipéptido y se acopla el siguiente aminoácido N-protegido.
Categorías destacadas
Ofrecemos una amplia gama de aminoácidos, resinas y reactivos de calidad inigualable, incluyendo Novabiochem®, para la síntesis de péptidos, química orgánica de alto rendimiento, péptidos marcados y productos fabricados a medida.
Nuestros ligandos y complejos NHC, estables y tolerables, pueden utilizarse como ligandos auxiliares eficaces para mantener el flujo de su trabajo en la investigación sobre catálisis organometálica y química catalítica.
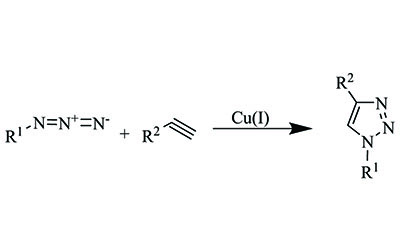
Nuestra cartera de reactivos químicos clic incluye una variedad de azidas, alquinos, catalizadores y ligandos para acelerar su progreso en biología química, química de polímeros, bioconjugación y descubrimiento de fármacos.
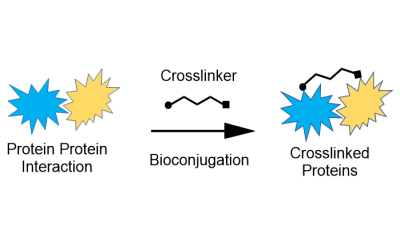
Nuestra cartera de enlazadores y reticulantes proporciona estabilidad estructural y fiabilidad en las interacciones proteína-proteína, proteína-péptido y péptido/proteína-molécula pequeña para todas sus necesidades de bioconjugación.
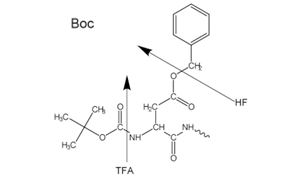
Figure 2Side-chain protecting groups for Boc solid-phase peptide synthesis (SPPS)
La síntesis de péptidos en fase sólida (SSPS) es el método más utilizado para la síntesis de péptidos debido a su eficiencia, simplicidad, rapidez y facilidad de paralelización. La SPPS consiste en la adición secuencial de residuos de aminoácidos protegidos y de cadenas laterales a un aminoácido o péptido unido a un soporte polimérico insoluble (Figura 1).
Para la protección N-α se utiliza un grupo Boc lábil al ácido (Boc SPPS) o un grupo Fmoc lábil a la base (Fmoc SPPS). Tras la eliminación de este grupo protector, se añade el siguiente aminoácido protegido utilizando un reactivo de acoplamiento o un derivado de aminoácido protegido preactivado. El aminoácido C-terminal se ancla a la resina mediante un enlazador, cuya naturaleza determina las condiciones necesarias para liberar el péptido del soporte tras la extensión de la cadena. Los grupos protectores de la cadena lateral se eligen a menudo de manera que se separen simultáneamente con el desprendimiento del péptido de la resina (figuras 2 y 3).
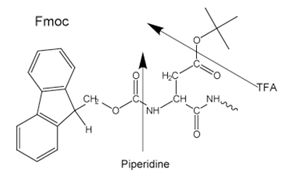
Figure 3.Side-chain protecting groups for Fmoc solid-phase peptide synthesis (SPPS)
La mayoría de los péptidos se preparan mediante el método Fmoc, ya que la escisión y desprotección finales se llevan a cabo mediante un tratamiento con ácido trifluoroacético, a diferencia del método Boc, que requiere el uso de HF anhidro líquido, altamente tóxico y corrosivo, en equipos especializados.
Se pueden preparar de forma rutinaria péptidos de 50 aminoácidos, aunque se suele informar de la síntesis de proteínas de más de 100 aminoácidos. Se pueden fabricar proteínas más largas mediante la ligación química nativa de péptidos totalmente desprotegidos en solución. Con este método, es posible sintetizar péptidos naturales que son difíciles de expresar en bacterias, incorporar aminoácidos no naturales o D-aminoácidos y generar péptidos cíclicos, ramificados, marcados y modificados postraduccionalmente.
La síntesis de péptidos en fase líquida, que suele utilizar protección Boc o Z-amino, ha sido sustituida por la síntesis de péptidos en fase sólida, excepto en los procesos existentes de síntesis a gran escala de péptidos con fines industriales.
Visite nuestro buscador de documentos para consultar fichas técnicas, certificados y documentación técnica.
Artículos relacionados
- Novabiochem® offers a wide range of linkers and derivatized resins for Fmoc solid-phase peptide synthesis with specialized protocols.
- Chromogenic and fluorogenic derivatives are invaluable tools for biochemistry, having numerous applications in enzymology, protein chemistry, immunology and histochemistry.
- Aspartimide formation 1,2 is caused by repeated exposure of aspartic acid-containing sequences to bases like piperidine and can result ultimately in the generation of 9 different by-products.
- Novabiochem® offers polymer supports for solid phase peptide synthesis, suitable for various peptide lengths and sequences.
- Long peptide purification removes impurities effectively, crucial for research and pharmaceutical applications.
- Ver todo (11)
Protocolos relacionados
- A guide to create solvent systems used for the thin-layer chromatography assay of Novabiochem products.
- Overcome challenges in synthesis and disulfide bond formation with protocols for Fmoc solid-phase peptide synthesis of peptides with cysteine and methionine.
- We provide an overview of our available reagents, together with recommendations and details of their use for synthesis of peptides containing post-translationally modified amino acids.
- Anhydrous HF is the preferred reagent for peptide cleavage from Boc-based resins, versatile and effective for various peptide synthesis.
- Fmoc resin cleavage and deprotection are crucial steps for peptide synthesis, yielding the desired peptide after resin detachment.
- Ver todo (7)
Encuentre más artículos y protocolos
¿Cómo podemos ayudarle?
Si tiene alguna pregunta, envíe una solicitud de asistencia al cliente
o hable con nuestro equipo de atención al cliente:
Correo electrónico custserv@sial.com
o llame al +1 (800) 244-1173
Asistencia adicional
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- Calculadoras y aplicaciones
Caja de herramientas de la página web: herramientas y recursos de investigación científica para química analítica, ciencias de la vida, síntesis química y ciencia de los materiales.
- Customer Support Request
Soporte al cliente que incluye ayuda con pedidos, productos, cuentas y problemas técnicos del sitio web.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.