Propiedades del agua, polaridad y función como disolvente universal
La molécula de agua
El agua es una molécula muy simple: está compuesta por dos átomos de hidrógeno combinados con un átomo de oxígeno. Sin embargo, es una molécula extraordinaria con varias propiedades excepcionales que la convierten en el disolvente más importante de la Tierra y esencial para la vida. El agua interviene en muchas reacciones bioquímicas, como la fotosíntesis y la respiración celular, y sirve como medio para transportar sustancias dentro y entre las células.
A pesar de su aparente simplicidad, el agua sigue siendo un importante objeto de curiosidad en la comunidad científica.
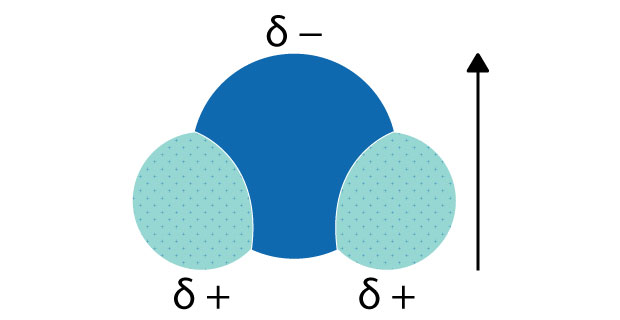
Figura 1. Polaridad de una molécula de agua.El átomo de oxígeno tiene una carga parcial negativa (δ-), mientras que los átomos de hidrógeno tienen cada uno una carga parcial positiva (δ+). El momento dipolar se representa mediante la flecha que va del lado positivo al negativo.
Polaridad del agua
Una molécula de agua tiene una forma curvada con un ángulo de 104,5 grados entre los dos átomos de hidrógeno, lo que provoca su polaridad. Aunque la molécula de agua no tiene carga, su átomo de oxígeno es más electronegativo que los átomos de hidrógeno (es decir, atrae más a los electrones). Como resultado, el lado de la molécula con el átomo de oxígeno tiene una ligera carga negativa, y cada uno de los átomos de hidrógeno tiene una ligera carga positiva. Una molécula con tal diferencia de carga se denomina dipolo (Figura 1).
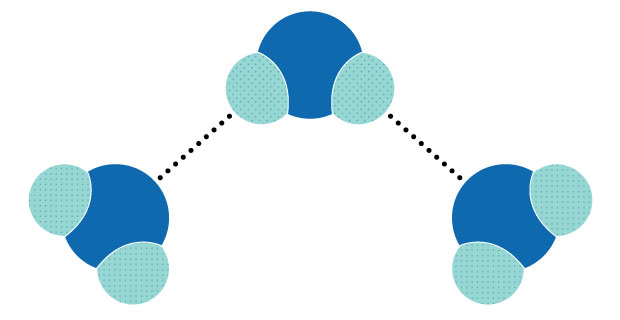
Figura 2. Enlace de hidrógeno de las moléculas de agua.
Los enlaces de hidrógeno y el agua
Este momento dipolar de las moléculas de agua hace que se atraigan entre sí (el lado del hidrógeno, ligeramente positivo, es atraído por el lado del oxígeno, ligeramente negativo) y por otras moléculas polares. Esta atracción se denomina enlace de hidrógeno (Figura 2).
Este enlace de hidrógeno es responsable de muchas de las propiedades únicas del agua, incluyendo el hecho de que el hielo tiene una densidad menor que el agua líquida, la alta tensión superficial y viscosidad del agua y, en cierta medida, la capacidad del agua para disolver muchas sustancias. Las altas temperaturas de fusión y ebullición del agua se deben a la energía necesaria para romper los enlaces de hidrógeno.
El agua es un excelente disolvente
El agua puede disolver más sustancias que cualquier otro líquido. Tiene una alta constante dieléctrica, lo que significa que puede reducir las fuerzas electrostáticas entre las partículas cargadas. Esto facilita la disociación de los compuestos iónicos en el agua. Es un excelente disolvente para las sales, ya que estas están formadas por iones con carga negativa y positiva que quedarán rodeados por las moléculas dipolares del agua (Figura 3).

Figura 3. Sal (cloruro de sodio) disuelta por moléculas de agua.
Las moléculas polares se disuelven fácilmente en el agua porque la parte positiva de la molécula polar es atraída por el átomo de oxígeno, mientras que la parte negativa es atraída por el átomo de hidrógeno. Además, el agua puede actuar tanto como ácido como base (es decir, es anfótera), lo que le permite interactuar con una amplia gama de sustancias. También es un buen disolvente para moléculas orgánicas neutras y establece enlaces de hidrógeno con muchas moléculas que intervienen en los procesos vitales, como los azúcares, las proteínas y los ácidos nucleicos.
Sin embargo, el agua no es realmente un disolvente universal, ya que no puede disolver moléculas hidrófobas o no polares.
Propiedades físico-químicas del agua
El agua tiene propiedades físico-químicas atípicas, como altos valores de viscosidad, tensión superficial y calor de vaporización. Esto se debe en gran medida a los enlaces de hidrógeno que conectan sus moléculas. A diferencia de la mayoría de las sustancias, el agua es menos densa en estado sólido (hielo) que en estado líquido.
En la tabla 1 se enumeran algunos parámetros clave del agua de alta pureza (ultrapura).
La molécula de agua tiene otra característica interesante: su capacidad para disociarse:
2 H2O ⇌ H3O+ + OH−
Esta capacidad de comportarse tanto como un ácido (donante de protones) como una base (aceptor de protones) es característica de las sustancias anfóteras. El método más común para especificar la acidez de una solución es su pH, que se define en términos de la concentración de iones de hidrógeno:
pH = −log [H+]
A menudo se plantean preguntas sobre el valor del pH del agua ultrapura y los intentos de medir el pH del agua ultrapura en los laboratorios a veces arrojan resultados desconcertantes. Consulte este artículo para obtener más información sobre el pH del agua ultrapura.
Póngase en contacto con nosotros si desea recibir ayuda de un experto en agua de laboratorio para seleccionar un sistema de agua para su laboratorio.
Productos relacionados
Para seguir leyendo, inicie sesión o cree una cuenta.
¿No tiene una cuenta?