Contaminantes del agua: tipos, fuentes e impacto en el laboratorio
El agua natural no es simplemente la molécula H2O. Contiene una variedad de compuestos disueltos que provienen de su contacto con la atmósfera, las rocas y el suelo, las plantas y los organismos vivos. Estas impurezas se clasifican normalmente como moléculas orgánicas, compuestos inorgánicos, microorganismos o bacterias y sus subproductos, partículas y coloides, y gases disueltos.
El agua potable del grifo se obtiene del agua natural y, por lo tanto, contiene estos compuestos, aunque los patrones gubernamentales suelen establecer concentraciones máximas de contaminantes nocivos. Aunque sea apta para el consumo, el agua del grifo puede contener compuestos que pueden afectar a los experimentos de laboratorio. Por este motivo, el agua debe purificarse aún más para que sea apta para análisis científicos sensibles.

Origen de las moléculas orgánicas en el agua
Las moléculas orgánicas disueltas presentes en el agua del grifo son principalmente de origen biológico. Por ejemplo, los ácidos húmicos, los taninos y los lignanos son subproductos de la descomposición de las plantas. Los contaminantes orgánicos artificiales también pueden estar presentes en el agua del grifo en niveles traza. Por ejemplo, cada vez se identifican más trazas de pesticidas, PFAS y productos farmacéuticos y de cuidado personal en el agua potable. Otro ejemplo es la liberación de plastificantes por las tuberías de PVC utilizadas para transportar y suministrar agua al grifo.
Impacto de los iones orgánicos en el laboratorio
El agua se puede utilizar para preparar soluciones y reactivos, para diluir patrones, en muchos métodos de preparación de muestras, como blanco, etc. Las sustancias orgánicas disueltas pueden afectar a técnicas como la HPLC, la UHPLC o la LC-MS, provocando inestabilidad en la línea de base, disminución de la sensibilidad y la resolución, picos fantasma y, finalmente, reduciendo la vida útil de la columna. Los cultivos celulares o los experimentos de biología molecular también pueden verse afectados por moléculas orgánicas específicas, que pueden interferir en el proceso de hibridación o actuar como disruptores endocrinos.
Eliminación de compuestos orgánicos del agua
Existen varias tecnologías de purificación que pueden eliminar las moléculas orgánicas del agua, entre ellas la ósmosis inversa (RO), el carbón activado o la fotooxidación con irradiación ultravioleta (UV).
Las impurezas orgánicas en el agua se controlan midiendo el carbono oxidable total (TOC, o carbono orgánico total). Para análisis de trazas orgánicas, se recomienda agua con un TOC muy bajo (5 ppb o menos).

Los iones inorgánicos que suelen estar presentes en el agua del grifo son cationes, como el sodio, el calcio, el magnesio y el hierro, y aniones, como el bicarbonato, el cloruro y el sulfato.
Origen de los iones en el agua
Muchos de los minerales que se encuentran en el agua del grifo provienen de la naturaleza y se originan en el suelo y las rocas con las que ha estado en contacto. Dependiendo de la fuente de agua, la composición de sales minerales del agua del grifo variará. Por ejemplo, en algunas zonas el agua se considera dura, lo que significa que contiene altos niveles de minerales disueltos, principalmente calcio y magnesio. El agua dura puede provocar la acumulación de incrustaciones en tuberías y electrodomésticos, y dejar manchas en la cristalería.
Impacto de los iones inorgánicos en el laboratorio
La presencia de iones, incluso en niveles traza, puede afectar a los análisis elementales e inorgánicos, provocando resultados inexactos o afectando a la sensibilidad experimental. Técnicas como la cromatografía iónica, la espectroscopia de absorción atómica (AAS) y la ICP-MS requieren agua libre de contaminación iónica. Además, los iones pueden afectar a las reacciones bioquímicas u orgánicas actuando como catalizadores o cofactores enzimáticos (por ejemplo, el magnesio en la PCR).
Eliminación de iones del agua
Existen varias tecnologías de purificación que pueden eliminar los iones del agua, entre ellas la ósmosis inversa (RO), las resinas de intercambio iónico y la desionización eléctrica (EDI).
Las impurezas iónicas del agua se controlan midiendo su conductividad eléctrica o resistividad. Una resistividad de 18,2 MΩ.cm indica que el agua está prácticamente libre de iones.
Las bacterias están presentes en el agua natural, especialmente en las aguas superficiales. Los patógenos responsables de las enfermedades transmitidas por el agua suelen eliminarse del suministro público de agua mediante cloración, ozonización o desinfección con rayos UV, pero el agua del grifo sigue conteniendo microorganismos vivos.
Impacto de las bacterias y sus subproductos en el laboratorio
Las bacterias pueden causar diferentes problemas en los experimentos de laboratorio, ya sea directamente o a través de sus subproductos, como endotoxinas, nucleasas, proteasas y fosfatasa alcalina. Se sabe que interfieren principalmente en los cultivos celulares, la biología molecular o los experimentos de inmunodetección, pero casi cualquier equipo de laboratorio se verá afectado por la proliferación de bacterias.
Eliminación del agua
Se pueden utilizar varias tecnologías para controlar los niveles de bacterias en el agua purificada. En primer lugar, la filtración a través de un filtro de malla de 0,22 µm o un ultrafiltro puede retener eficazmente las bacterias. Además, se puede utilizar la irradiación con luz UV para inactivar las bacterias. Los subproductos bacterianos (endotoxinas, nucleasas, proteasas o fosfatasa alcalina) son mucho más pequeños que las bacterias y solo se pueden eliminar mediante ultrafiltración.

Origen de las partículas en el agua
El agua natural suele contener partículas blandas (como restos vegetales) y partículas duras (arena, polvo), así como coloides (sílice, hierro coloidal u óxido de aluminio, arcilla). También pueden proceder de minerales que se precipitan cuando el agua se expone al oxígeno (por ejemplo, carbonato cálcico o magnésico).
Impacto de las partículas y los coloides en el laboratorio
Las partículas en suspensión y los coloides pueden causar turbidez, lo que afecta a cualquier método que utilice haces de luz (por ejemplo, la espectrofotometría). Pueden obstruir los filtros o depositarse en las líneas, columnas o recipientes de los instrumentos, lo que obliga a realizar limpiezas o mantenimientos frecuentes.
Las partículas y los coloides pueden interferir en el funcionamiento de los instrumentos. Por ejemplo, las partículas pueden dañar las bombas e inyectores de HPLC y aumentar la contrapresión del sistema. También pueden interferir en la medición y el análisis de micro y nanopartículas, microplásticos, etc.
Eliminación del agua
Para la mayoría de las aplicaciones, una filtración de 0,22 µm es adecuada para eliminar las partículas del agua purificada. En situaciones específicas (cuando se realizan análisis ICP-MS o se analizan micro o nanopartículas), puede ser necesaria una filtración adicional. En estas situaciones, se pueden recomendar filtros específicos (0,1 µm o ultrafiltros).

La mayoría de los gases disueltos en el agua natural se absorben del aire ambiente. Los cambios de temperatura y presión atmosférica pueden afectar a la disolución de los gases. El agua a nivel del mar, al estar sometida a una presión más alta, contiene más gases que el agua a mayor altitud.
El agua del grifo contiene gases disueltos como nitrógeno, oxígeno y dióxido de carbono. El oxígeno, por ejemplo, se absorbe de la atmósfera o puede ser producido por las plantas acuáticas. El dióxido de carbono puede ser generado por organismos acuáticos o por la fermentación microbiana de la materia orgánica. Otros gases como el argón, el nitrógeno, el metano o el sulfuro de hidrógeno pueden estar presentes, pero normalmente solo en niveles traza. Algunos gases también pueden ser generados por la actividad humana (agrícola o industrial).
Impacto de los gases disueltos en el laboratorio
La concentración de oxígeno en el agua puede afectar a determinadas reacciones bioquímicas. Los gases disueltos pueden formar burbujas que son perjudiciales para procesos como el recuento de partículas o las mediciones espectrofotométricas. También pueden obstruir los tubos pequeños.
Eliminación del agua
Los sistemas de purificación de agua de sobremesa rara vez incluyen un desgasificador, y la desgasificación, si es necesaria, se suele realizar por separado, justo antes de utilizar el agua.
Incluso sin un desgasificador, el agua ultrapura recién purificada con una resistividad de 18,2 MOhm.cm solo contiene niveles muy bajos de CO2. Esto se debe a que el CO2 está en equilibrio con el ácido carbónico, el carbonato y el bicarbonato en el agua (Figura 1), que se eliminan eficazmente mediante tecnologías de desionización. Sin embargo, el agua ultrapura absorberá rápidamente el CO2 del aire si se deja reposar.
Contaminación del agua purificada durante el almacenamiento
Cuando se almacena, el agua ultrapura absorbe rápidamente cualquier contaminación presente en el aire del laboratorio.
En un experimento clásico, se dejó agua ultrapura con una resistividad de 18,2 MΩ.cm a 25 °C en un vaso de precipitados y se midió la evolución de su resistividad a lo largo del tiempo. Los resultados se muestran en la figura 1 y demuestran la rápida contaminación del agua por el dióxido de carbono del aire, lo que provoca la producción de HCO3- en el agua y la consiguiente disminución de la resistividad de 18,2 MΩ.cm a 4 MΩ.cm en aproximadamente una hora.
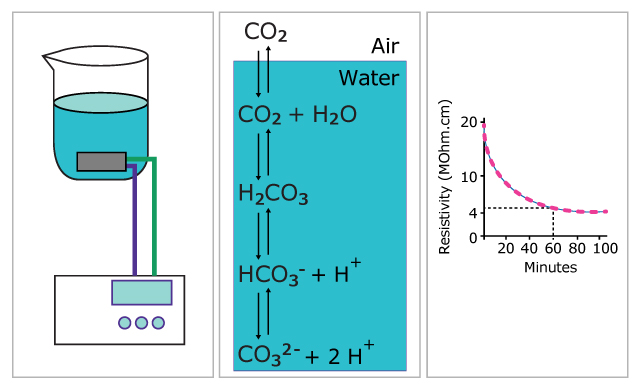
Figura 1.Demostración de la contaminación del agua ultrapura con dióxido de carbono del aire.
Lo que es válido para el dióxido de carbono también lo es para otras sustancias químicas que pueden estar presentes en el aire de un laboratorio, como los vapores ácidos (del ácido nítrico o del ácido clorhídrico) y los disolventes volátiles (como el tolueno, la acetona o el tetrahidrofurano). El agua purificada también se contamina fácilmente con materiales extraídos de los recipientes, como el sodio y la sílice del vidrio, los plastificantes y los ionenes de los materiales poliméricos (por ejemplo, los ésteres de ftalato de las tuberías de PVC, el fluoruro de las tuberías de PTFE) y los ionenes metálicos de los recipientes metálicos.
Por este motivo, para minimizar los riesgos de contaminación y la variabilidad experimental que pueden causar estos contaminantes, el agua ultrapura debe producirse justo antes de su uso y utilizarse lo antes posible.
Póngase en contacto con nosotros si desea recibir ayuda de un experto en agua de laboratorio para seleccionar un sistema de agua para su laboratorio.
Productos relacionados
Para seguir leyendo, inicie sesión o cree una cuenta.
¿No tiene una cuenta?