Contaminants de l'eau : types, sources et impacts en laboratoire
L'eau naturelle n'est pas simplement composée de molécules H2O. Elle contient divers composés dissous provenant de son contact avec l'atmosphère, les roches et le sol, les plantes et les organismes vivants. Ces impuretés sont généralement classées en molécules organiques, composés inorganiques, micro-organismes ou bactéries et leurs sous-produits, particules et colloïdes, et gaz dissous.
L'eau potable du robinet est fabriquée à partir d'eau naturelle et contient donc ces composés, bien que les étalons gouvernementaux fixent généralement des concentrations maximales pour les contaminants nocifs. Même si elle est potable, l'eau du robinet peut contenir des composés susceptibles d'avoir un impact sur les expériences en laboratoire. C'est pourquoi l'eau doit être purifiée davantage pour pouvoir être utilisée dans des analyses scientifiques sensibles.

Origine des molécules organiques dans l'eau
Les molécules organiques dissoutes présentes dans l'eau du robinet sont principalement d'origine biologique. Par exemple, les acides humiques, les tanins et les lignanes sont des sous-produits de la décomposition des plantes. Des contaminants organiques d'origine humaine peuvent également être présents à l'état de traces dans l'eau du robinet. Par exemple, des traces de pesticides, de PFAS et de produits pharmaceutiques et de soins personnels sont de plus en plus souvent identifiées dans l'eau potable. Un autre exemple est le rejet de plastifiants par les tuyaux en PVC utilisés pour transporter et acheminer l'eau jusqu'au robinet.
Impact des ions organiques en laboratoire
L'eau peut être utilisée pour préparer des solutions et des réactifs, pour diluer des étalons, dans de nombreuses méthodes de préparation d'échantillons, comme blanc, etc. Les matières organiques dissoutes peuvent affecter des techniques telles que la HPLC, l'UHPLC ou la LC-MS en provoquant une instabilité de la ligne de base, une diminution de la sensibilité et de la résolution, des pics fantômes et, à terme, une réduction de la durée de vie de la colonne. Les cultures cellulaires ou les expériences de biologie moléculaire peuvent également être affectées par des molécules organiques spécifiques, qui peuvent interférer avec le processus d'hybridation ou agir comme des perturbateurs endocriniens.
Élimination des composés organiques de l'eau
Plusieurs technologies de purification permettent d'éliminer les molécules organiques de l'eau, notamment l'osmose inverse (RO), le charbon actif ou la photo-oxydation par irradiation ultraviolette (UV).
Les impuretés organiques présentes dans l'eau sont contrôlées en mesurant le carbone oxydable total (COT, ou carbone organique total). Pour les analyses de traces organiques, il est recommandé d'utiliser de l'eau à très faible teneur en COT (5 ppb ou moins).

Les ions inorganiques couramment présents dans l'eau du robinet sont des cations, tels que le sodium, le calcium, le magnésium et le fer, et des anions, tels que le bicarbonate, le chlorure et le sulfate.
Origine des ions dans l'eau
La plupart des minéraux présents dans l'eau du robinet proviennent de la nature et sont issus du sol et des roches avec lesquels elle a été en contact. La composition en sels minéraux de l'eau du robinet varie en fonction de la source d'approvisionnement. Par exemple, dans certaines régions, l'eau est considérée comme dure, ce qui signifie qu'elle contient des niveaux élevés de minéraux dissous, principalement du calcium et du magnésium. L'eau dure peut entraîner l'accumulation de tartre dans les tuyaux et les appareils électroménagers, et laisser des traces sur la verrerie.
Impact des ions inorganiques en laboratoire
La présence d'ions, même à l'état de traces, peut affecter les analyses élémentaires et inorganiques en faussant les résultats ou en affectant la sensibilité des expériences. Des techniques telles que la chromatographie ionique, la spectroscopie d'absorption atomique (AAS) et l'ICP-MS nécessitent une eau exempte de contamination ionique. De plus, les ions peuvent affecter les réactions biochimiques ou organiques en agissant comme catalyseurs ou cofacteurs enzymatiques (par exemple, le magnésium dans la PCR).
Élimination des ions de l'eau
Plusieurs technologies de purification permettent d'éliminer les ions de l'eau, notamment l'osmose inverse (RO), les résines échangeuses d'ions et l'électrodéionisation (EDI).
Les impuretés ioniques présentes dans l'eau sont contrôlées en mesurant sa conductivité électrique ou sa résistivité. Une résistivité de 18,2 MΩ.cm indique que l'eau est presque exempte d'ions.
Les bactéries sont présentes dans l'eau naturelle, en particulier dans les eaux de surface. Les agents pathogènes responsables des maladies d'origine hydrique sont généralement éliminés des réseaux publics d'approvisionnement en eau par chloration, ozonation ou désinfection aux UV, mais l'eau du robinet contient encore des micro-organismes vivants.
Impact des bactéries et de leurs sous-produits en laboratoire
Les bactéries peuvent causer différents problèmes dans les expériences de laboratoire, soit directement, soit par le biais de leurs sous-produits, tels que les endotoxines, les nucléases, les protéases et la phosphatase alcaline. Elles sont connues pour interférer principalement avec les cultures cellulaires, la biologie moléculaire ou les expériences d'immunodétection, mais presque tous les équipements de laboratoire sont affectés par la prolifération des bactéries.
Élimination de l'eau
Plusieurs technologies peuvent être utilisées pour contrôler les niveaux de bactéries dans l'eau purifiée. Tout d'abord, la filtration à travers un filtre à mailles de 0,22 µm ou un ultrafiltre permet de retenir efficacement les bactéries. En outre, l'irradiation aux rayons UV peut être utilisée pour inactiver les bactéries. Les sous-produits bactériens (endotoxines, nucléases, protéases ou phosphatase alcaline) sont beaucoup plus petits que les bactéries et ne peuvent être éliminés que par ultrafiltration.

Origine des particules dans l'eau
L'eau naturelle contient généralement des particules molles (telles que des débris végétaux) et des particules dures (sable, poussière) ainsi que des colloïdes (silice, fer colloïdal ou oxyde d'aluminium, argile). Elles peuvent également provenir de minéraux qui précipitent lorsque l'eau est exposée à l'oxygène (par exemple, le carbonate de calcium ou de magnésium).
Impact des particules et des colloïdes en laboratoire
Les particules en suspension et les colloïdes peuvent provoquer une turbidité, affectant toute méthode reposant sur des faisceaux lumineux (par exemple, la spectrophotométrie). Ils peuvent obstruer les filtres ou se déposer dans les conduites, les colonnes ou les conteneurs des instruments, ce qui nécessite des nettoyages ou des entretiens fréquents.
Les particules et les colloïdes peuvent interférer avec le fonctionnement des instruments. Par exemple, les particules peuvent endommager les pompes et les injecteurs HPLC et augmenter la contre-pression du système. Elles peuvent également interférer avec la mesure et l'analyse des micro et nanoparticules, des microplastiques, etc.
Élimination de l'eau
Pour la plupart des applications, une filtration de 0,22 µm est suffisante pour éliminer les particules de l'eau purifiée. Dans certaines situations spécifiques (lors de la réalisation d'analyses ICP-MS ou de l'analyse de micro- ou nanoparticules), une filtration supplémentaire peut être nécessaire. Dans ces situations, des filtres spécifiques (0,1 µm ou ultrafiltres) peuvent être recommandés.

La plupart des gaz dissous dans l'eau naturelle sont absorbés à partir de l'air ambiant. Les changements de température et de pression atmosphérique peuvent avoir une incidence sur la dissolution des gaz. L'eau au niveau de la mer, soumise à une pression plus élevée, contient plus de gaz que l'eau à des altitudes plus élevées.
L'eau du robinet contient des gaz dissous tels que l'azote, l'oxygène et le dioxyde de carbone. L'oxygène, par exemple, est absorbé dans l'atmosphère ou peut être produit par les plantes aquatiques. Le dioxyde de carbone peut être généré par des organismes aquatiques ou par la fermentation microbienne de matières organiques. D'autres gaz tels que l'argon, l'azote, le méthane ou le sulfure d'hydrogène peuvent être présents, mais généralement seulement à l'état de traces. Certains gaz peuvent également être générés par l'activité humaine (agricole ou industrielle).
Impact des gaz dissous en laboratoire
La concentration en oxygène dans l'eau peut affecter certaines réactions biochimiques spécifiques. Les gaz dissous peuvent former des bulles qui nuisent à des processus tels que le comptage de particules ou les mesures spectrophotométriques. Ils peuvent également obstruer les petits tubes.
Élimination de l'eau
Les systèmes de purification d'eau de paillasse comprennent rarement un dégazeur, et le dégazage, s'il est nécessaire, est généralement effectué séparément, juste avant l'utilisation de l'eau.
Même sans dégazeur, l'eau ultra-pure fraîchement purifiée avec une résistivité de 18,2 MOhm.cm ne contient que de très faibles niveaux de CO2. En effet, le CO2 est en équilibre avec l'acide carbonique, le carbonate et le bicarbonate dans l'eau (figure 1), qui sont efficacement éliminés par les technologies de déionisation. Cependant, l'eau ultra-pure absorbe rapidement le CO2 de l'air si elle est laissée au repos.
Contamination de l'eau purifiée pendant le stockage
Lorsqu'elle est stockée, l'eau ultra-pure absorbe rapidement toute contamination présente dans l'air du laboratoire.
Dans une expérience classique, de l'eau ultra-pure d'une résistivité de 18,2 MΩ.cm à 25 °C a été laissée dans un bécher et l'évolution de sa résistivité a été mesurée au fil du temps. Les résultats sont présentés dans la figure 1 et démontrent la contamination rapide de l'eau par le dioxyde de carbone présent dans l'air, entraînant la production de HCO3- dans l'eau et la diminution consécutive de la résistivité de 18,2 MΩ.cm à 4 MΩ.cm en environ une heure.
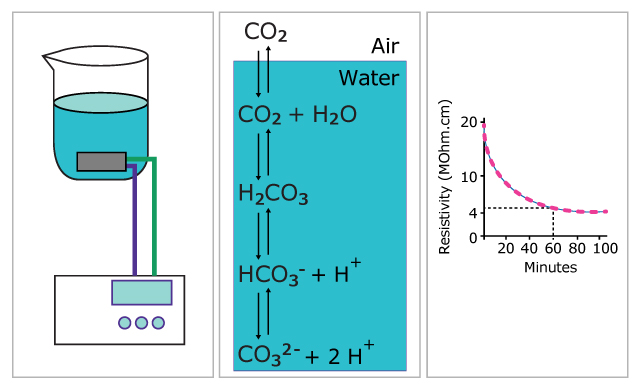
Figure 1.Démonstration de la contamination de l'eau ultra-pure par le dioxyde de carbone présent dans l'air.
Ce qui vaut pour le dioxyde de carbone vaut également pour d'autres substances chimiques pouvant être présentes dans l'air d'un laboratoire, telles que les vapeurs acides (provenant de l'acide nitrique ou chlorhydrique) et les solvants volatils (tels que le toluène, l'acétone ou le tétrahydrofurane). L'eau purifiée est également facilement contaminée par des substances extraites des récipients, telles que le sodium et la silice du verre, les plastifiants et les ions des matériaux polymères (par exemple, les esters de phtalate des tuyaux en PVC, le fluorure des tuyaux en PTFE) et les ions métalliques des récipients métalliques.
Pour cette raison, afin de minimiser les risques de contamination et la variabilité expérimentale pouvant être causés par ces contaminants, l'eau ultra-pure doit être produite juste avant son utilisation et utilisée dès que possible.
Contactez-nous si vous souhaitez bénéficier de l'aide d'un expert en eau de laboratoire pour choisir un système d'eau adapté à votre laboratoire.