Propriétés de l'eau, polarité et rôle en tant que solvant universel
La molécule d'eau
L'eau est une molécule très simple : elle est composée de deux atomes d'hydrogène combinés à un atome d'oxygène. Pourtant, c'est une molécule extraordinaire qui possède plusieurs propriétés exceptionnelles qui en font le solvant le plus important sur Terre et un élément essentiel à la vie. L'eau intervient dans de nombreuses réactions biochimiques, notamment la photosynthèse et la respiration cellulaire, et sert de moyen de transport des substances à l'intérieur et entre les cellules.
Malgré son apparente simplicité, l'eau reste un sujet de curiosité important pour la communauté scientifique.
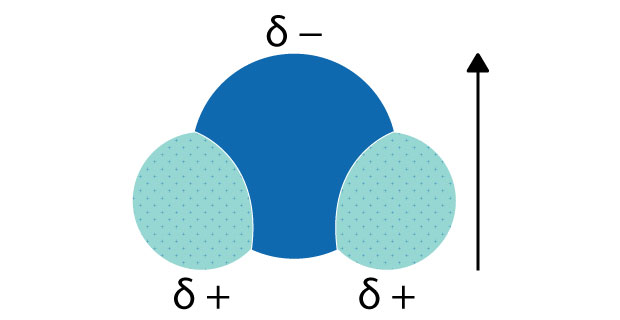
Figure 1. Polarité d'une molécule d'eauL'atome d'oxygène possède une charge partielle négative (δ-), tandis que les atomes d'hydrogène possèdent chacun une charge partielle positive (δ+). Le moment dipolaire est représenté par la flèche allant du côté positif vers le côté négatif.
Polarité de l'eau
Une molécule d'eau a une forme courbée avec un angle de 104,5 degrés entre les deux atomes d'hydrogène, ce qui lui confère sa polarité. Bien que la molécule d'eau n'ait pas de charge, son atome d'oxygène est plus électronégatif que les atomes d'hydrogène (c'est-à-dire qu'il attire davantage les électrons). Par conséquent, le côté de la molécule où se trouve l'atome d'oxygène a une légère charge négative, et chacun des atomes d'hydrogène a une légère charge positive. Une molécule présentant une telle différence de charge est appelée dipôle (figure 1).
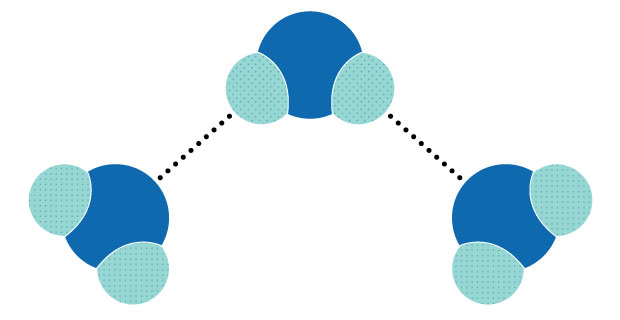
Figure 2. Liaison hydrogène entre les molécules d'eau.
Liaison hydrogène et eau
Ce moment dipolaire des molécules d'eau les amène à s'attirer les unes les autres (le côté hydrogène légèrement positif est attiré par le côté oxygène légèrement négatif) et à s'attirer d'autres molécules polaires. Cette attraction est appelée liaison hydrogène (figure 2).
Cette liaison hydrogène est responsable de nombreuses propriétés uniques de l'eau, notamment le fait que la glace a une densité inférieure à celle de l'eau liquide, la tension superficielle et la viscosité élevées de l'eau et, dans une certaine mesure, la capacité de l'eau à dissoudre de nombreuses substances. Les températures élevées de fusion et d'ébullition de l'eau sont dues à l'énergie nécessaire pour rompre les liaisons hydrogène.
L'eau est un excellent solvant
L'eau peut dissoudre plus de substances que tout autre liquide. Elle possède une constante diélectrique élevée, ce qui signifie qu'elle peut réduire les forces électrostatiques entre les particules chargées. Cela facilite la dissociation des composés ioniques dans l'eau. C'est un excellent solvant pour les sels, car ceux-ci sont constitués d'ions chargés négativement et positivement qui seront entourés par les molécules d'eau dipolaires (figure 3).

Figure 3. Sel (chlorure de sodium) dissous par des molécules d'eau.
Les molécules polaires se dissolvent facilement dans l'eau car la partie positive de la molécule polaire est attirée par l'atome d'oxygène, tandis que la partie négative est attirée par l'atome d'hydrogène. De plus, l'eau peut agir à la fois comme un acide et comme une base (c'est-à-dire qu'elle est amphotère), ce qui lui permet d'interagir avec un large éventail de substances. C'est également un bon solvant pour les molécules organiques neutres et elle établit des liaisons hydrogène avec de nombreuses molécules impliquées dans les processus vitaux, telles que les sucres, les protéines et les acides nucléiques.
Cependant, l'eau n'est pas réellement un solvant universel, car elle ne peut pas dissoudre les molécules hydrophobes ou non polaires.
Propriétés physico-chimiques de l'eau
L'eau possède des propriétés physico-chimiques atypiques, telles qu'une viscosité, une tension superficielle et une chaleur de vaporisation élevées. Cela s'explique en grande partie par les liaisons hydrogènes qui relient ses molécules. Contrairement à la plupart des substances, l'eau est moins dense à l'état solide (glace) qu'à l'état liquide.
Certains paramètres clés de l'eau de haute pureté (ultra-pure) sont répertoriés dans le tableau 1.
La molécule d'eau possède une autre caractéristique intéressante : sa capacité à se dissocier :
2 H2O ⇌ H3O+ + OH−
Cette capacité à se comporter à la fois comme un acide (donneur de protons) et comme une base (accepteur de protons) est caractéristique des substances amphotères. La méthode la plus courante pour déterminer l'acidité d'une solution est son pH, qui est défini en fonction de la concentration en ions hydrogène :
pH = −log [H+]
Des questions sont souvent soulevées quant à la valeur du pH de l'eau ultra-pure et les tentatives de mesure du pH de l'eau ultra-pure en laboratoire donnent parfois des résultats déroutants. Reportez-vous à cet article pour plus d'informations sur le pH de l'eau ultra-pure.
Contactez-nous si vous souhaitez bénéficier de l'aide d'un expert en eau de laboratoire pour choisir un système d'eau adapté à votre laboratoire.