オリゴヌクレオチドの定量化
オリゴヌクレオチドの定量化について
オリゴヌクレオチドの定量化とは、短い一本鎖または二本鎖の核酸(DNA、RNA)のポリマーであるオリゴヌクレオチドの濃度を溶液中で決定するプロセスのことです。この測定は、分子生物学、バイオテクノロジー、臨床診断におけるさまざまなアプリケーションに欠かせません。
正確で信頼できるオリゴヌクレオチド定量化のための一般的な注意点とヒント
- サンプルは適切に希釈する:高濃度オリゴヌクレオチド溶液は、定量化法(UV分光法など)の直線範囲に入るように希釈して、飽和を回避し、正確な測定値を確保します。
- 純度と夾雑物を明らかにする:吸光度比(A260/A280)を測定して、オリゴヌクレオチドの純度を評価します。吸光度比がDNAで約1.8、RNAで約2.0であれば、サンプルの純度が高いことが分かりますが、それ以外の場合はタンパク質やその他の夾雑物によるコンタミネーションがある可能性が示唆されます。
- 正しい吸光係数を使用する:260 mnにおける吸光度に基づいて濃度を算出する場合には、正しい吸光係数を使用してください。この係数は、ヌクレオチドの特定の配列や組成に応じて異なります。
- コンタミネーションを避ける:ヌクレアーゼフリー水ときれいなガラス器具を使用して、定量化の正確さに影響を及ぼすコンタミネーションを回避します。塩類や有機化合物などの夾雑物は、吸光度測定値に干渉します。
- オリゴヌクレオチドは適切に保管する:オリゴヌクレオチド溶液は、推奨温度(通常-20°Cまたは-80°C)で保管し、分解や不正確な定量化を引き起こす凍結融解を繰り返さないようにします。
- 蛍光ベースの方法の使用を検討する:低濃度サンプルの場合には、UV吸光度法より感度が高く、低濃度のオリゴヌクレオチドの検出が可能な蛍光ベースの定量化法の使用を検討します。
ヌクレオチドの定量化方法
波長260 nmの紫外線(UV)で照射すれば、溶液中の核酸濃度は分光光度計によって簡単に定量化することができます(図1)。この手法が可能なのは、核酸塩基が紫外吸光の仕方がそれぞれ異なる共役二重結合を形成しているためです。

図1.分光光度計内での吸光試料セル溶液中の核酸は、波長260 nmの入射紫外光により最大強度で照射を受ける。核酸中の塩基が紫外光線の一部を吸収するため、透過紫外光線は強度が低下する。吸光度は、以下の計算式によって求められる。
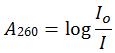
ただし: A260 = 260 nmにおける吸光度、Io = 入射光強度、I = 透過光強度。
吸光量と吸光核酸濃度の関係はランベルト・ベールの法則により、以下のように示されます。
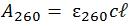
ただし:
A260 = 260 nmにおける吸光度
260 = 260 nmにおけるオリゴヌクレオチドの吸光係数(L ⋅ mol-1 ⋅ cm-1)
c = 濃度(mol L-1)
ℓ = 光路長(cm)
ランベルト・ベールの法則において重要なのは、紫外光が入射してから透過する間に、塩基がどの程度光を吸収したかということの指標となる吸光係数です。各塩基の吸光度は異なるため、定量分析の対象となっている核酸の最終的な吸光度は、組成塩基、塩基配列および配列長によって変わります。したがって、最も正確な結果を得る方法は、オリゴヌクレオチドごとに吸光係数を算出することです。最近接塩基対モデル(nearest-neighbor model)による算出がオリゴヌクレオチドには最も適しており、その計算式は以下のようになります。
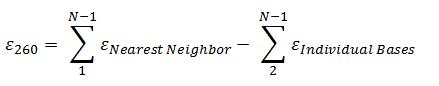
表1および表2 は、最近接塩基対法を使ってオリゴヌクレオチドの最終的な吸光係数の和を算出する際に用いる、最近接塩基対および個々の塩基の吸光係数を示すものです。
なお、試料セルの光路長は1.0 cmです。ランベルト・ベールの法則の数式に代入する数値がこれですべて揃いました。
濃度計算の際、ランベルト・ベールの法則の数式は、以下のように変形できます。
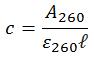
例:5'-ACGT-3'の定量
ステップ 1:吸光係数を計算する
260 = (AC+CG+GT)-(C+G) L ⋅ mol-1 ⋅ cm-1
260 = (21,200+18,000+20,000)-(7,400+11,500) L ⋅ mol-1 ⋅ cm-1
260 = 40,300 L ⋅ mol-1 ⋅ cm-1
上記の計算で得た「40,300」という値は、多くの技術ウェブサイトおよび技術文書で「40.3」と表示されます。これは単位がL ⋅ mmol-1 ⋅ cm-1 であるためです(モルではなくミリモルを使用していることに注意)。
ステップ 2:濃度を計算する
A260 は光学密度(OD)単位で1.0とします。
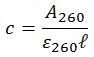
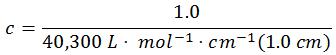
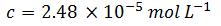
ステップ 3:モル質量を計算する
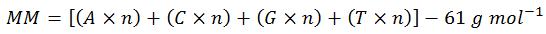
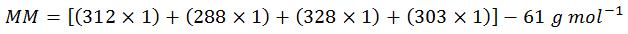
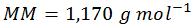
通常は「モル質量」の代わりに「分子量」という言葉を使いますが、今回の計算では1モル当たりの質量についての単位が必要なので、正しくは「モル質量」となります。また、表示の簡略化のため、上に示した各塩基のモル質量は1の位で四捨五入してあります。したがって、示されている1,170という値は実際の計算結果である1,173.83よりも若干小さくなっています。
ステップ 4:濃度の単位を慣用的な単位に変換する
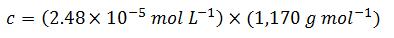
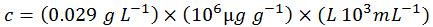
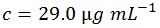
したがって、今回の5'-ACGT-3'という配列の分子については、1 OD = 29.0 µg mL-1 (1 ODとは、光路長1.0 cmの時に A260 = 1.0となる溶液1 mL中に含まれるオリゴヌクレオチドの量)となります。私たちのオリゴヌクレオチド配列オンライン計算ツールであるOligoEvaluator™ を使って得られた値を、比較のために以下に示します。
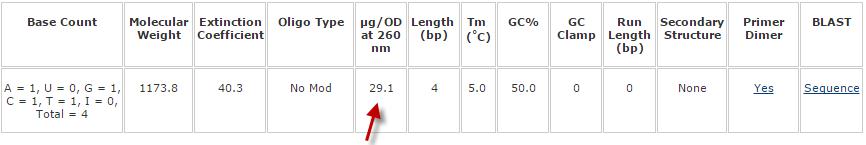
上記のように手で計算した29.0という値と、OligoEvaluator™によって算出された29.1という値はほぼ一致しています(少し差がありますが、これは上記ステップ3で説明した通り、手で計算した際に四捨五入したモル質量を用いたことによるものです)。
この5'-ACGT-3'という配列のオリゴヌクレオチドについては、OligoEvaluator™だけでなく、テクニカルデータシートでも29.1という値が表示されます。
5'-ACGT-3'の計算の簡易化
ここまで説明した計算手順は長くて煩雑です。以下の計算式は、全ステップを一つにまとめたもので、簡易的な計算が可能です。
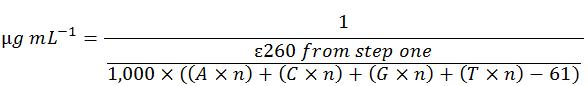
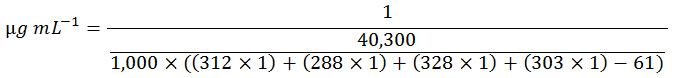
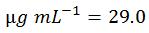
修飾
スタンダードオリゴヌクレオチドと修飾されたオリゴヌクレオチドの濃度計算における唯一の違いは、修飾分子のモル質量が考慮されて、オリゴヌクレオチドの合計モル質量に加えられるということです。ここまで例として示してきた配列は以下のとおりです。
● 5'-ACGT-3'
を以下のように変えたとします。
● 5'-6-FAM™-ACGT-3'
この場合、長い計算手順または簡易版計算式のいずれかに1,711.3 g mol-1 という新たなモル質量の値を代入すれば値を算出できます。
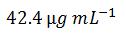
これは、OligoEvaluator™によって得られる値と合致します。

簡便的な換算
過去の実験から以下の簡便的な換算が可能であることが実証されています(ただし、「ds」および「ss」はそれぞれ「二本鎖」および「一本鎖」の略)。
● A260 dsDNA = 50 µg mL-1
● A260 ssDNA = 37 µg mL-1
● A260 ssRNA = 40 µg mL-1
一切計算をしなくても、これらの変換係数を使えば、(二本鎖DNAについての推定の場合)ゲノムDNA断片など、より配列が長くA、C、GおよびTという各塩基の分布が均一な場合については、ある程度正確な推定値を示すことができます。しかし、オリゴヌクレオチドの場合は、組成塩基が偏っている可能性が高いため、こうした推定値の信頼性は低くなります(実際よりも高い濃度推定値が出ることが多い)。オリゴヌクレオチドごとに、上に示した長い計算手順または簡易版計算式のいずれかを使って濃度を判断しなければなりません。長い計算手順または簡易版計算式のいずれを使っても、テクニカルデータシートに示されている定量分析値を検証することができます。