밀리셀® 행잉 인서트를 이용한 대장 오가노이드 단일층 배양
오가노이드 유래 단일층 배양의 개요 및 장점
투과성 인서트에서 배양된 오가노이드 유래 단층 배양(2.5차원 세포 배양으로도 알려짐)은 3차원 오가노이드 모델과 보다 전통적인 2차원 체외 방법 사이의 간극을 메웁니다. 환자 조직 유래(PDO) 또는 유도만능줄기세포(iPSC)에서 유래된 오가노이드는 생리학적으로 관련성이 높은 모델을 제공하여 원발성 상피 조직을 밀접하게 모방합니다. 투과성 인서트 위에서 오가노이드를 단층으로 배양함으로써 연구자들은 전상피 전기 저항(TEER) 측정에 유리한 균일하고 잘 정의된 상피층을 구축할 수 있습니다.
기존 단층 배양에 비해 오가노이드 유래 단층 배양은 여러 장점을 제공합니다. 강화된 장벽 특성을 보이며, 더 단단한 접합부와 향상된 TEER을 통해 장벽 무결성을 더 정확하게 평가할 수 있습니다. 또한 오가노이드는 세포 다양성을 유지하여 생체 상피 조직의 복잡성을 더 잘 재현합니다. 투과성 막 인서트에서 배양된 오가노이드 유래 단층 배지는 정밀한 실험 조작 및 측정을 가능하게 하여 약물 흡수 메커니즘, 질병 병리학, 장내 미생물군과의 상호작용 연구를 용이하게 합니다. 본 연구에서는 Millicell® 24-well 매달린 세포 배양 인서트에서 배양된 오가노이드 유래 단층 배지의 생성, 최적화 및 평가에 대한 포괄적인 지침을 제시합니다.
관련 제품
오가노이드 유래 단일층 생성
iPSC 유래 대장 오가노이드(SCC300)의 단일 세포 분해
본 단일 세포 분해 실험에는 Millicell® 24-well 매달린 인서트(PTRP24H48)를 사용하였으며, 인서트당 세포 밀도는 2x10⁵ 세포였습니다. 인서트는 1X PBS에 용해된 2% GFR Matrigel®로 코팅하여 37°C에서 최소 1시간 또는 4°C에서 하룻밤 동안 처리하였습니다.
참고: 분해 프로토콜 시작 전에 인서트를 코팅하십시오. 본 프로토콜은 hiPSC 유래 대장 오가노이드(SCC300) P21 6일차, 2 x 10 cm 접시에서 채취한 120 x 25 µL 돔을 기준으로 합니다. Accumax (SCR006) 및 1X PBS와 같은 모든 시약에 10 µM의 1X ROCKi (SCM075)를 첨가하십시오.
- 10mL 피펫을 사용하여 10mL의 차가운 1X PBS+1X ROCKi에서 120 x 25 µL 돔을 분리하고 분해하십시오.
- 오가노이드 현탁액 2.5 mL를 4개의 50 mL 원추형 튜브(50 mL 원추형 튜브당 30-40 x 25 µL 돔)에 각각 옮기고, 현탁액을 측면에 5-10회 부딪혀 Matrigel® 돔에서 오가노이드를 더 분리합니다.
- 각 튜브를 얼음처럼 차가운 1X PBS+1X ROCKi로 30mL까지 채우고 2000 rpm (872 x g)에서 10분간 원심 분리합니다.
- 상층액을 조심스럽게 제거하고, 4개의 50mL 원추형 튜브에 있는 각 침전물을 5mL의 얼음처럼 차가운 1X PBS+1X ROCKi로 재현탁시킵니다.
- 2개의 50 mL 원뿔형 튜브에 있는 현탁액을 15 mL 원뿔형 튜브로 모읍니다. 나머지 2개의 50 mL 튜브에 있는 현탁액도 동일한 방법으로 처리합니다. 참고: 이 단계에서 현탁액을 15 mL 원뿔형 튜브로 옮기면 침전물 일부를 잃지 않으면서 잔여 Matrigel®을 제거하는 데 도움이 됩니다.
- 2000 rpm (872 x g)에서 10분간 원심분리하고, 2개의 15 mL 원추형 튜브 각각에서 상층액을 조심스럽게 흡입 제거합니다. 참고: 흡입 피펫에 P-200 팁을 부착하여 펠릿에서 가능한 한 많은 Matrigel®을 제거하도록 합니다.
- 각 펠릿을 4mL의 Accumax+1X ROCKi로 4회 위아래로 피펫팅하여 재현탁시킨 후, 두 개의 펠릿을 하나의 튜브에 합치십시오(총 8mL의 Accumax+1X ROCKi).
- 튜브 측면에 4~6회 부딪혀 현탁액을 추가로 재현탁합니다.
- 튜브를 37°C, 5% CO2 인큐베이터에 10분간 넣습니다. 5분 간격으로 튜브를 꺼내 후드로 옮긴 후, 각 튜브 벽에 8~10회 피펫팅하여 현탁액을 재현탁시킵니다.
- 튜브를 인큐베이터에 다시 넣고 5분간 두십시오.
- 인큐베이터에서 튜브를 꺼내 튜브 측면에 대해 8~10회 더 피펫팅합니다.
- 현미경으로 세포 현탁액 10µL를 관찰하여 단일 세포 분리가 이루어졌는지 확인합니다. 참고: 10분 배양은 일부 작은 덩어리와 함께 단일 세포를 얻기에 충분합니다.
- 현탁액을 50mL 원뿔형 튜브로 옮겨 모으십시오.
- 세포 현탁액이 담긴 50mL 원추형 튜브에 얼음처럼 차가운 1X PBS + 1X ROCKi 25mL를 추가하고 2000rpm 또는 872 x g에서 10분간 원심 분리합니다.
- 상층액을 제거하고 세포 침전물을 3 mL의 3dGRO® Human Colon Organoid Expansion Medium (SCM304) + Penicillin/Streptomycin (P/S) + 1X ROCKi에 5 mL 피펫으로 6~8회 위아래로 피펫팅하여 재현탁시킵니다.
- 세포 계수기(예: Scepter 3.0)에서 세포 수를 측정하기 위해 50µL의 세포를 취합니다.
- 필요한 경우 세포를 원심 분리합니다. SCM304 + P/S + 1X ROCKi로 세포를 1x106 세포/mL로 재현탁합니다.
- 1x10⁶ 세포/mL 및 0.5x10⁶ 세포/mL 농도의 세포 샘플 두 개를 추가로 준비하고 배양 접시에 접종하십시오.
a. 2x10⁶ 세포/mL 농도의 세포 200µL를 2% GFR Matrigel®으로 사전 코팅된 인서트 각각에 접종하여 인서트당 400k 세포를 배양하십시오.
b. 사전 코팅된 2% GFR Matrigel® 인서트 각각에 1x10⁶ 세포/mL 농도의 세포 200 µL를 접종하여 인서트당 200k를 확보합니다.
c. 사전 코팅된 2% GFR Matrigel® 인서트 각각에 0.5x106 세포/mL 농도의 세포 200 µL를 접종하여 인서트당 100k를 처리합니다.
- 인서트의 기저측 각 웰에 성장 배지 + 1X ROCK 억제제 1000 µL를 첨가합니다.
- 접시를 37°C, 5% CO2 인큐베이터에 넣어 배양합니다.
- 인서트에 시드된 세포를 현미경으로 매일 관찰하여 단층의 접합 상태를 확인합니다.
- 시드 1일 후 3D 및 2D 세포 배양용 생사 검출 키트(CBA415)를 사용하여 생사 검출 염색을 수행합니다.
- 단층 배양이 100%에 도달할 때까지 SCM304+P/S+1X ROCKi로 2일마다 배지를 교체합니다.
- 단층 배양이 완료되기 하루 전부터 원하는 시점에 도달할 때까지 매일 조직 배양 후드에서 TEER 측정을 수행하십시오. 사용 전 TEER 기기 설정에 대해서는 제조사의 지침을 참조하십시오.
대장 PDO(SCC321) 단일 세포 분해
본 단일 세포 분해 실험에는 Millicell® 24-well hanging inserts (PTRP24H48)를 사용하였으며, 인서트당 세포 밀도는 2x10⁵ 세포였습니다. 인서트는 1X PBS에 용해된 2% GFR Matrigel®로 코팅하여 37°C에서 최소 1시간 또는 4°C에서 하룻밤 동안 배양했습니다. 본 프로토콜은 배양 5일차 대장 환자 유래 오가노이드(PDO)(SCC321)의 50-60 x 10 µL 돔을 기준으로 합니다. TrypLE Express 및 1X PBS와 같은 모든 시약에 1X ROCKi(SCM075)를 첨가하십시오.
- 냉각된 1X PBS+1X ROCKi 용액에서 P-1000 피펫을 사용하여 Matrigel® 돔을 여러 번 분리하고 분쇄합니다.
- 오가노이드 현탁액을 3개의 15mL 원뿔형 튜브(15mL 원뿔형 튜브당 최대 20 x 10 µL 돔)로 옮기고, 현탁액을 측면에 여러 번 부딪혀 Matrigel® 돔에서 오가노이드를 더 분리합니다. 참고: 60 x 10 µL 돔보다 많은 경우, 추가 15mL 튜브를 사용하십시오.
- 4°C에서 2000 rpm (872 x g)으로 10분간 원심분리합니다.
- 상층액을 조심스럽게 흡입 제거하고, 3개의 15mL 원추형 튜브에 담긴 각 펠릿을 5mL의 얼음처럼 차가운 1X PBS+1X ROCKi에 재현탁시킵니다.
- 2000 rpm (872 x g)에서 4°C로 10분간 원심 분리합니다.
- 상층액을 조심스럽게 제거하고, 3개의 15mL 원추형 튜브에 각각의 펠릿을 2mL TrypLE Express+1X ROCKi로 재부유시킵니다. 현탁액이 매우 점성이 높으면 TrypLE Express를 더 추가합니다.
- 37°C 인큐베이터에서 10분간 배양하고, 10분마다 피펫으로 각 튜브의 측면에 여러 번 부딪혀 재현탁합니다.
- 현미경으로 현탁액 내 단일 세포를 확인합니다. 2-3개 세포로 구성된 소규모 군집만 존재해야 합니다. 오가노이드가 여전히 분해되지 않았다면 37°C에서 배양을 계속하고 5분마다 분해 상태를 확인합니다.
- 오르가노이드가 분해되면, 세포 현탁액에 냉각된 DMEM/F-12 PLUS 배지(SCM162) + 1X ROCK 억제제 또는 1X PBS + 1X ROCK 억제제 5mL를 첨가합니다.
- 세포 현탁액을 500 x g에서 5분간 원심 분리합니다.
- 상층액을 제거하고 세포 펠릿 위에 남아 있는 Matrigel® 층을 조심스럽게 제거합니다.
- 세포 펠릿을 성장 배지(SCM105) + 1X ROCK 억제제에 1x105 세포/mL의 농도로 재현탁하고, 세포 덩어리를 분해하기 위해 여러 번 위아래로 피펫팅합니다.
- 300 µL의 성장 배지에 2x105 세포/인서트를 시드합니다.
- 인서트의 기저면 측 각 웰에 배양 배지 + 1X ROCK 억제제 1000 µL를 첨가합니다.
- 플레이트를 5% CO2가 있는 37°C 인큐베이터에 넣어 배양합니다.
- 삽입물에 접종된 세포의 단층 밀집도를 현미경으로 매일 관찰합니다.
- 시드 1일 후, 3D 및 2D 세포 배양용 생사 생존도 분석 키트(CBA415)를 사용하여 생사 생존도 염색을 수행하십시오.
- 단층 배양이 100%에 도달할 때까지 SCM304+P/S+1X ROCKi로 2일마다 배지를 교체합니다.
- 단층 배양이 완료되기 하루 전부터 원하는 시점에 도달할 때까지 매일 조직 배양 후드에서 TEER 측정을 수행하십시오. 사용 전 TEER 기기 설정에 대해서는 제조사의 지침을 참조하십시오.
Millicell® 인서트 코팅을 위한 GFR Matrigel® 최적 비율 결정
이 단일 세포 분해 실험에서는 Greiner CELLSTAR® 24-well plate (M8812)용 1 µm 기공 크기의 Millicell® 24-well hanging inserts (PTRP24H48)를 사용했으며, 인서트당 (24-well) 세포 밀도는 200k 세포였습니다. 인서트는 1X PBS에 1%, 2%, 4%, 6%, 8% 또는 10% GFR Matrigel®로 코팅되었습니다.
- 밀리셀® 인서트를 코팅하기 위해 얼음처럼 차가운 1X PBS 또는 DMEM/F-12 Plus (SCM162)에 1%, 2%, 4%, 6%, 8% 및 10% GFR Matrigel®을 준비합니다. 참고: 희석액은 사용 직전까지 얼음에 보관하십시오.
- 무균 기법을 사용하여 밀리셀® 행잉 인서트를 블리스터 포장에서 꺼내 24-웰 세포 배양 플레이트에 넣으십시오.
- 희석된 GFR Matrigel®을 얼음에서 꺼내 조직 배양 후드로 옮깁니다.
- 적절한 인서트에 200-400 µL의 희석된 GFR Matrigel®을 첨가하고, 세포를 시드하기 전에 최소 1시간 동안 37°C 인큐베이터에 두거나 냉장고에서 하룻밤 동안 보관하십시오.
a. Millicell® 인서트에 세포를 시드하기 위해 Accumax를 사용하여 iPSC
유래 오가노이드(SCC300)를 단일 세포 분해하는 방법은 상기 프로토콜을 참조하십시오. b. Millicell® 인서트에 세포를 시드하기 위해 TrypLE Express를 사용하여 환자 유래 오가노이드(SCC321)를 단일 세포 분해하는 방법은 상기 프로토콜을 참조하십시오.
밀리셀® 인서트 상의 오가노이드 유래 단일층에 대한 생사 세포 생존율 염색
- "스피로이드 및 오가노이드 배양 프로토콜" 섹션에 명시된 3D 및 2D 세포 배양용 생사 세포 생존율 분석 키트(CBA415) 사용 염색 프로토콜을 따르십시오.
- 습도 조절된 37°C 인큐베이터에서 24-웰 인서트 플레이트를 꺼냅니다.
- 필터가 부착되지 않은 P-200 팁이 부착된 흡입 피펫을 사용하여 정점 쪽에서 배지를 조심스럽게 흡입합니다. 참고: 인서트(단층)의 표면을 긁지 않도록 주의하십시오.
- 12mL 용액(배지 1:1 1X PBS) 당 칼세인 AM 5µL, 프로피디움 요오드 20µL, 호에스트 33342 8µL를 첨가합니다.
- 염색 용액을 완전히 혼합하기 위해 보텍스합니다.
- 인서트의 단층 배양을 1X PBS로 두 번 세척합니다.
- 세포 단층이 있는 각 인서트에 200-400 µL의 염색 용액을 첨가하고 37°C에서 60분 동안 배양합니다.
- 염색 용액을 1X PBS로 교체하고 적절한 여기 및 방출 필터를 사용하여 형광 현미경으로 이미지를 촬영합니다.
- 계속 배양할 세포의 경우 배지로 두 번 세척한 후 신선한 배지로 교체합니다.
- 접시를 다시 습도 조절된 37°C 인큐베이터에 넣어 배양을 계속하십시오.
Millicell® 인서트 상에서의 단일층 형성 모니터링
인서트에 시드된 세포를 현미경으로 매일 관찰하여 단일층의 융합도를 확인하고, 단일층이 융합되기 하루 전부터 매일 조직 배양 후드에서 TEER 측정을 시작합니다. 사용 전 TEER 기기 설정을 위해 제조사의 지침을 참조하십시오.
Millicell® 인서트 상의 단일층 분화
- 단층이 100% 융합에 도달했을 때만 분화를 시작하십시오.
- ENR 분화 배지 조성을 사용하여 단층을 분화시키려면 인서트(정상면)에 300 µL, 웰(기저면)에 1000 µL를 첨가하십시오.
- 매체는 이틀에 한 번씩 교체하십시오.
- 실험의 원하는 종결점에 도달할 때까지 매일 또는 격일로 TEER 측정을 계속하십시오.
Millicell® 인서트 상의 단층 배양 세포에 대한 ICC 염색 및 이미징
- 원하는 시점에 37°C, 5% CO2 인큐베이터에서 단층을 제거하여 조직 배양 후드에 놓으십시오.
- 흡입 피펫을 사용하여 각 인서트의 정단면(apical side)과 기저측면(basolateral side, 웰)에서 배지를 흡입 제거하십시오. 팁: 필터가 없는 P-200 팁을 흡입 피펫 끝에 부착하거나 마이크로피펫을 사용하여 정단면과 기저측면에서 배지를 천천히 흡입 제거하십시오. 이 단계 및 이후 단계에서 인서트의 막 표면을 긁지 않도록 주의하십시오.
- 0.4mL의 1X PBS로 정단면을, 1mL의 1X PBS로 기저측면을 각각 한 번씩 세척합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫으로 정점 및 기저측면에서 1X PBS를 천천히 흡입 제거하십시오.
- 각 24-웰 인서트를 1X PBS에 용해된 4% 파라포름알데히드 0.4mL로 실온에서 30분간 고정합니다.
- P-1000 피펫으로 4% 파라포름알데히드를 제거하고 적절히 폐기하십시오.
- 첨단면은 0.4mL, 기저측면은 1mL의 1X PBS로 두 번 세척합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫으로 정단 및 기저 측면의 1X PBS를 천천히 흡입 제거합니다.
- 각 단층을 1X PBS에 용해된 0.3% Triton-X-100 + 1% BSA 용액 200-400 µL로 15분간 투과 처리합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫을 사용하여 정단면에서 천공화 용액을 천천히 흡입 제거합니다.
- 차단 용액(1X PBS + 5% 일반 당나귀 혈청 + 1% BSA) 0.4mL를 실온에서 1시간 또는 4°C에서 하룻밤 동안 첨가합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫을 사용하여 정단면에서 차단 완충액을 천천히 흡입 제거합니다. 이 과정에서 인서트 표면을 긁지 않도록 주의하십시오.
- 1차 비결합 또는 결합 항체 0.2-0.4 mL를 희석 완충액(1X PBS 내 1% BSA)에 용해하여 실온에서 2-4시간 또는 4°C에서 하룻밤 동안 흔들어 주면서 인서트를 염색합니다.
- P-1000 피펫으로 각 인서트마다 팁을 교체하며 염색 용액을 제거합니다.
- 각 인서트를 1X PBS로 5분씩 3회 세척합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫으로 정점 측의 1X PBS를 천천히 흡입하여 제거합니다. 이 과정에서 인서트 표면을 긁지 않도록 주의하십시오.
- 필요한 경우, 희석 완충액(1X PBS에 1% BSA)에 적절한 2차 항체를 사용하여 실온에서 2~3시간 또는 4°C에서 하룻밤 동안 흔들어 주면서 인서트를 염색합니다.
- 각 인서트를 1X PBS로 5분씩 3회 세척합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫을 사용하여 정점면에서 1X PBS를 천천히 흡입 제거하십시오. 이 과정에서 인서트 표면을 긁지 않도록 주의하십시오.
- 실온에서 15분간 1X PBS에 용해된 2-10 µg/mL 농도의 DAPI 용액 0.2-0.4 mL로 대조 염색합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫을 사용하여 정단면에서 DAPI 용액을 천천히 흡입 제거합니다. 이 과정에서 삽입물의 표면을 긁지 않도록 주의하십시오.
- 1X PBS로 한 번 세척합니다.
- 필터가 없는 P-200 팁이 부착된 흡입 피펫으로 정단면에서 1X PBS를 천천히 흡입 제거합니다. 이 과정에서 인서트 표면을 긁지 않도록 주의하십시오.
- 첨단면에 1X PBS 0.4mL를, 기저 측면에 1X PBS 1mL를 첨가합니다. 4°C에서 보관하십시오.
- 플레이트에서 인서트를 직접 촬영하거나, 인서트를 조심스럽게 잘라내어 유리 바닥 플레이트에 장착합니다.
오가노이드 배양의 규모 확대
PDO 대장 오가노이드(SCC321)는 배양 후 5~7일, hiPSC 유래 대장 오가노이드(SCC300)는 10일이 경과한 후 배양 접종이 가능합니다. 단일 세포 분리와 Millicell® 인서트 시딩을 위한 최적의 수확 시기는 대수 성장기입니다: SCC321의 경우 5일차, SCC300의 경우 7일차입니다. 일반적으로 대수 성장기는 배양이 분화 준비가 되기 약 2-3일 전이지만, 개별 오가노이드 시스템에 따라 다를 수 있습니다.
다음으로, 특정 수의 오가노이드 돔에서 단일 세포의 예상 수율을 결정하십시오. 각 돔 내 오가노이드 점유율을 매번 분화 시 일관되게 유지하는 것이 권장됩니다. 마지막으로, 3~4일차에 100% 접합도를 달성하기 위해 Millicell® 24-well 매달린 세포 배양 인서트(PTRP24H48)에 접종해야 하는 단일 세포 수를 결정합니다. 이후 Millicell® 24-well 매달린 세포 배양 인서트에 필요한 오가노이드 돔의 총 수를 계산할 수 있습니다(표 1).
|
수확에 최적의 시기 | 예상 수율 | 인서트당 필요한 오가노이드 돔 수 | 24개 인서트에 필요한 오가노이드 돔 수 |
|---|---|---|---|---|
PDO 대장 |
5일차 |
~10 x 10µL 돔으로 434k 세포 생산 |
200k/삽입물 (~5 x 10µL 돔)
|
24개의 인서트에 약 120 x 10µL 돔 필요 |
hiPSC-대장 |
7일차 |
~25 x 10µL 돔으로 525k 세포 생산 |
인서트당 200k (~10 x 10µL 돔) |
24개의 인서트에 대해 약 240 x 10µL 돔 |
표 1: PDO 대장 오가노이드(SCC321) 및 hiPSC 유래 대장 오가노이드(SCC300) 수확 및 시딩 가이드라인
분리 및 삽입체에 세포 배양
분리 최적 시간은 단일 세포 현탁액을 생성하는 가장 짧은 배양 시간입니다. SCC321의 경우 TrypLE로 20~30분 배양이 가장 효과적이며, SCC300의 경우 Accumax(SCR006)로 약 10분 배양이 가장 효과적임을 확인했습니다(그림 1). SCC321 세포를 TrypLE Express로 20~30분 배양하면 단일 세포 분리가 가능하며, 삽입체당 200k 세포를 접종하면 4일차에 완전한 단일층을 형성합니다.
최적화된 접종 밀도는 SCC321 및 SCC300 모두 3~5일 사이에 융합 단일층을 형성하는 200k 세포/인서트를 달성하는 것입니다(그림 1).

그림 1. 분해 시약 및 배양 기간 비교. A. SCC300 세포를 삽입물당 200k 세포 농도로 TrypLE Express와 15분간 배양했으나 5일차까지 완전한 단층 배양을 형성하지 못함. B. SCC300 세포를 삽입물당 200k 세포 농도로 TrypLE Express와 45분간 배양했으나 5일차까지 완전한 단일층을 형성하지 못했다. C. SCC300 세포를 37°C에서 Accumax와 10분간 배양하는 것만으로도 단일 세포 분리가 가능했다. 200k 세포/인서트로 시드한 경우 5일차에 융합 단일층을 생성했습니다.
인서트 코팅에 최적의 Matrigel® 비율을 결정하는 것은 오가노이드 유래 단층 세포 배양의 성공적 생성에 매우 중요합니다. 2% 및 4% GFR Matrigel®로 코팅된 인서트를 테스트한 결과, GFR Matrigel®의 비율이 너무 높으면 단층이 융합에 도달하는 데 더 오랜 시간이 걸리고, 단층 두께가 고르지 않으며, 3D 구조가 생성될 수 있음을 발견했습니다(그림 2B).
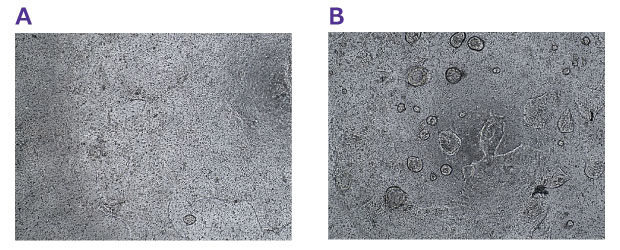
그림 2: 100k로 시드된 hiPSC-대장 오가노이드 배양을 위한 삽입체 코팅에 최적의 GFR Matrigel® 비율 결정. A. 2% GFR Matrigel®이 8일차까지 융합 단일층 형성에 가장 효과적이었다. B. 4% GFR Matrigel®은 8일차까지 멤브레인 삽입체 상에 3차원 구조 형성으로 이어졌다.
단일 세포 현탁액을 Millicell® 인서트에 접종한 지 24시간 후, Live-Dead Cell Viability Assay Kit (CBA415)를 사용하여 세포 생존율을 측정할 수 있습니다. 인서트 상의 약 85-90%의 세포는 생존 세포를 나타내는 칼세인-AM(녹색)으로 녹색으로 염색되는 반면, 아주 적은 비율의 세포는 프로피디움 요오드화물(PI)(사멸 세포, 적색)로 염색됩니다(그림 3).
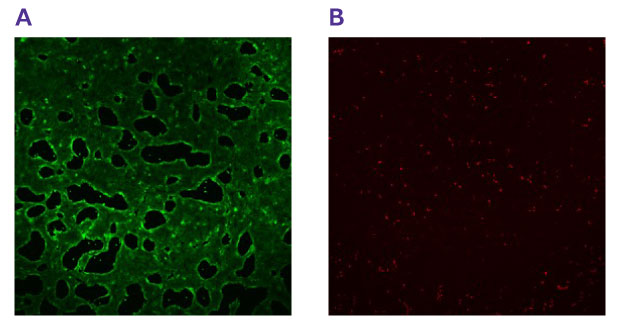
그림 3: 삽입체 상의 시드 후 세포 생존율. A. 칼세인-AM(녹색)으로 염색된 멤브레인 삽입체 상의 hiPSC 대장 세포(SCC300). 이는 생존 세포를 나타냄. B. PI(사멸 세포, 적색)로 염색된 멤브레인 삽입체 상의 세포. 단층 배양은 이미징 전 1X PBS로 두 번 세척함.
단일층 형성 및 분화
확장 배지에서 배양된 오가노이드는 증식 세포가 풍부하고, 점액세포, 장상피세포, 장내분비세포와 같은 분화된 세포 유형이 적습니다. EGF, 노긴(Noggin), R-스폰딘(R-Spondin)을 함유한 분화 배지(ENR)에서 배양된 오가노이드는 증식 세포가 덜 풍부하고 성숙한 세포 유형의 비율이 더 높습니다. 이러한 성숙한 세포 유형은 장 내벽에서 장벽 역할을 하여 출입을 조절하는 단단한 접합부(tight junctions) 형성에 중요합니다(그림 4).
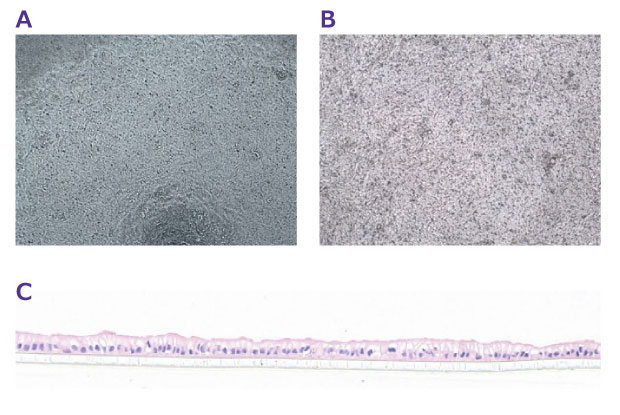
그림 4. Millicell® 인서트 상의 융합된 오가노이드 유래 단일층의 대표적 이미지. A. SCC321 세포를 200k 세포/인서트 농도로 접종한 후 4일차의 명시야 이미지. B. SCC300 세포를 200k 세포/인서트 농도로 접종한 후 3일차의 명시야 이미지. C. 12일차 오가노이드 단일층의 헤마톡실린-에오신 염색.
SCC321은 ENR 배지에서 분화 기간 9일 이상이 소요되어 최대 TEER 측정에 도달한 반면, SCC300은 ENR 배지에서 8-9일, 3dGRO® 인간 대장 오가노이드 확장 배지(SCM304)에서 11-12일이 소요되어 최대 TEER 측정에 도달했습니다.
오가노이드 유래 단일층 세포 배양에서의 TEER 평가
TEER 측정은 장 내벽과 같은 상피 세포층의 완전성과 밀착성을 평가합니다. 이 방법은 일반적으로 Millicell® ERS 3.0 볼토옴미터(MERS03000)와 같은 상피 볼토옴미터를 사용하며, 이는 Millicell® 행잉 인서트(PTRP24H48)와 같은 투과성 지지 막 위에 배양된 상피 세포층에 걸쳐 저수준의 전류를 가합니다.
PDO 대장 오가노이드(SCC321)와 hiPSC 유래 대장 오가노이드(SCC300)에 대해 매일 수행한 TEER 측정은 각각 3일차와 4일차에 접합 상태에 도달했습니다. 배양은 확장 배지(SCC321의 경우 3dGRO® L-WRN Conditioned Media Supplement (SCM105), SCC300의 경우 3dGRO® 인간 대장 오가노이드 확장 배지 (SCM304)) 또는 분화 배지(ENR)에서 유지되었습니다. ENR에서 배양된 대장 PDO(SCC321) 단층은 TEER 값이 지속적으로 증가한 반면, L-WRN에서 배양된 단층은 이러한 추세를 유지하지 못했습니다(그림 5A). 반면, iPSC 유래 대장 오가노이드(SCC300) 단층 배양은 SCM304 배지 또는 ENR 배지에서 배양되었는지 여부와 관계없이 TEER 값이 꾸준히 증가하는 모습을 보였습니다(그림 5B).
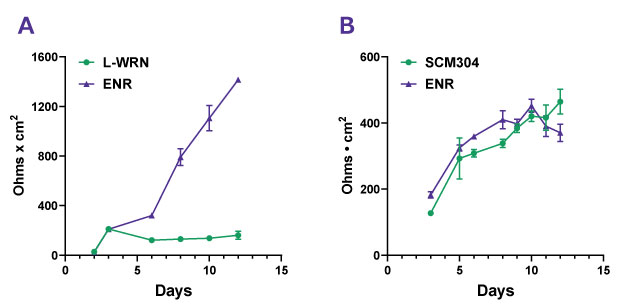
그림 5. Millicell® 인서트(PTRP24H48)에서 12일간 배양된 오가노이드 유래 단층 세포의 TEER 측정 결과. A. 환자 유래 대장 오가노이드(SCC321)를 접종하여 확장 배지에서 3일간 배양하였다. 4일차에 단층 배양을 포함한 Millicell® 인서트는 분화 배지(ENR)로 전환하거나 확장 배지(L-WRN)에서 유지했다. B. 인간 iPSC 유래 대장 오가노이드(SCC300)를 접종한 후 접종 3일째부터 3dGRO® 인간 대장 오가노이드 확장 배지(SCM304) 또는 분화 배지(ENR)에서 배양했습니다.
이러한 차이는 iPSC 유래 대장 오가노이드에서 관찰된 더 성숙한 표현형에 기인할 수 있습니다. 상대적 유전자 발현 분석 결과, 대장 PDO에 비해 iPSC 유래 대장 오가노이드에서 크로모그라닌 A(CHGA) 및 MUC2 뮤신의 발현 수준이 더 높게 나타났습니다(그림 6). 이러한 결과는 iPSC 유래 대장 오가노이드가 특화된 세포 계통을 보유하는 반면, 대장 PDO의 경우 ENR 배지를 통한 추가 분화가 필요함을 시사합니다.
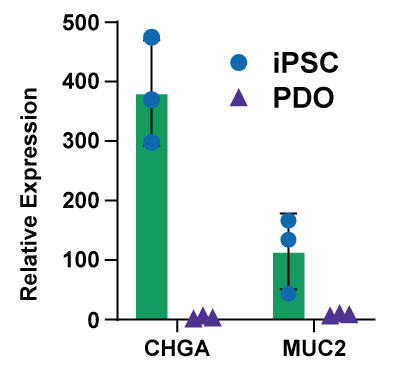
그림 6. 확장 배지(L-WRN)에서 배양된 대장 PDO와 비교한 iPSC 유래 대장 오가노이드에서 크로모그라닌 A(CHGA) 및 MUC2 뮤신의 RNAseq 상대적 유전자 발현.
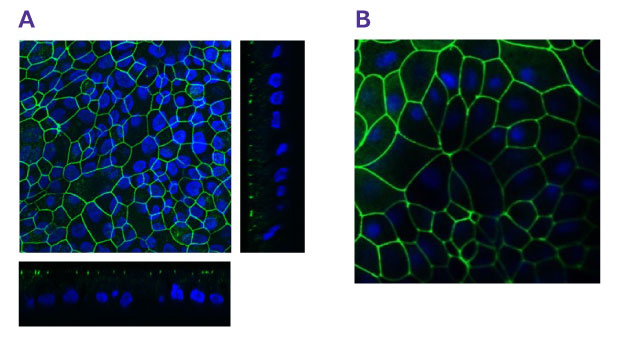
TEER 값의 상승은 완전한 밀착 연결과 최소한의 세포간 투과성을 특징으로 하는 강력한 상피 장벽을 의미합니다. 이는 정단단 접합 단백질 ZO-1이 정단부에 국한되어 존재하는 것과 관련이 있습니다. 대장 PDO(SCC321) 및 iPSC 유래 대장 오가노이드(SCC300) 단층 배양에서의 ZO-1 면역형광 염색은 단백질의 적절한 정단부 국소화를 보여주었습니다(그림 7).
밀리셀® 인서트 코팅 및 시드 배양을 위한 팁과 요령
- 흡입 피펫의 팁에 필터가 없는 P-200 팁을 부착하거나 P-200 피펫을 사용하여 인서트에서 PBS를 천천히 흡입 제거하십시오. 인서트 표면을 긁지 않도록 주의하십시오.
- GFR Matrigel® 농도는 모델 시스템에 따라 최적화해야 할 수 있습니다. 막 표면에 3차원 구조가 형성되면 Matrigel® 비율을 줄이는 것을 고려하십시오.
- 배양 중 세포 생존율을 높이기 위해 분해 시약에 10 µM ROCK 억제제를 첨가하십시오(상기 분해 프로토콜 참조).
- 단일 세포 현탁액을 200k 세포/24-웰 인서트에 접종하여 3-4일 내에 완전한 단일층을 형성하도록 합니다.
- Greiner 24-well 배양 플레이트(M8812) 내 Millicell® 24-well 인서트의 정점측(apical side)에는 300 µL, 기저측(basolateral side)에는 1000 µL를 사용하십시오. 최적의 기저측 용량은 플레이트 브랜드에 따라 다릅니다. 권장 배지 용량에 대한 자세한 내용은 Millicell® 인서트 사용자 가이드에서 확인할 수 있습니다.