Pruebas de pirógenos
Las pruebas de detección de pirógenos son un paso fundamental para garantizar la seguridad de los productos médicos administrados por vía parenteral, como los productos farmacéuticos o biofarmacéuticos. Forma parte de las pruebas de liberación obligatorias para evitar reacciones febriles potencialmente mortales inducidas por sustancias pirógenas. La prueba de activación de monocitos (MAT) puede detectar tanto endotoxinas como pirógenos no endotoxinas en una sola prueba in vitro.
Desde julio de 2025, la MAT es el método de elección según la Farmacopea Europea para la detección de endotoxinas y no endotoxinas, en sustitución de la prueba de pirógenos en conejo (RPT)
.
Products
Prueba de Activación Monocitaria (MAT)
Utilizada para detectar tanto endotoxinas como pirógenos no endotoxinas en productos parenterales, tales como productos farmacéuticos y dispositivos médicos, la MAT ofrece una& nbsp;alternativa a las pruebas in vitro.nbsp;in vitro alternativa a los ensayos convencionales con animales de acuerdo con las directrices reglamentarias.
La prueba de pirógenos en conejos y la prueba de lisado de amebocitos de Limulus (LAL) se utilizan ampliamente para la detección de pirógenos. Ambos métodos utilizan animales y presentan algunas limitaciones. La prueba de pirógenos en conejos muestra una falta de solidez, ya que una reacción animal puede diferir mucho de una reacción humana. En el ensayo LAL, solo se detectan endotoxinas, lo que provoca un riesgo para la seguridad al ignorar pirógenos no endotoxinas que podrían estar presentes en la muestra analizada.
Para superar estas limitaciones, el ensayo de activación de monocitos (MAT) se introdujo en la Farmacopea Europea en 2010 como método de compendio para sustituir al ensayo de pirógenos en conejos (EP Capítulo 2.6.30) y mencionado en la guía de la FDA para la industria.
Nota:
La Comisión de la Farmacopea Europea tomó la decisión de poner fin a la prueba de pirógenos en conejo de acuerdo con el principio de las 3Rs considerando que la TMA es la mejor opción alternativa.
;A partir de julio de 2025, la prueba de pirógenos en conejo (TMA) está prohibida en Europa y se ha suprimido el capítulo general 2.6.8 sobre la prueba de pirógenos en conejo.
PyroMAT® prueba in vitro prueba para detectar pirógenos endotoxinas y no endotoxinas
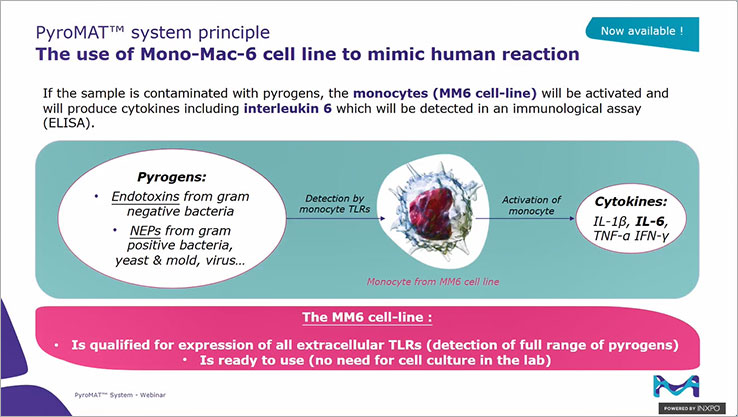
El sistema PyroMAT® se basa en la línea celular Mono-Mac-6 y la lectura de IL-6. Ofrece todas las ventajas de la prueba de activación de monocitos combinadas con los beneficios de utilizar una línea celular.
- Detección de una amplia gama de pirógenos:< la seguridad del paciente está garantizada si se analiza toda la gama de pirógenos. Al igual que la prueba de pirógenos en conejos (RPT), la MAT es eficaz para la detección de pirógenos tanto endotoxinas como no endotoxinas.
- Ampliación de la gama de productos que pueden analizarse:< los métodos aplicados con más frecuencia, RPT, prueba de endotoxinas bacterianas (BET) o LAL, están limitados en cuanto a los tipos de productos que pueden analizar. The MAT offers more flexibility regarding its applications.
- In vitro assay that mimics the human immune reaction: for a robust predictive model that reduces animal consumption.
- Cumplimiento de las normativas y directrices internacionales:< en línea con las tendencias éticas de la industria y las autoridades reguladoras para disminuir el uso de pruebas basadas en animales.
- Reactividad estandarizada y alta sensibilidad (LOD 0,05 EU/mL).< La comodidad de una línea celular lista para usar reduce el laborioso trabajo de laboratorio y evita la necesidad de un laboratorio de cultivo celular.
- Células cualificadas:
Además de ser citadas en la validación internacional de MAT, las células Mono-Mac-6 están cualificadas para la expresión de todos los receptores Toll-Like (TLR) de superficie para garantizar la detección de una amplia gama de pirógenos.
- Las células Mono-Mac-6 están cualificadas para la expresión de todos los receptores Toll-Like (TLR) de superficie para garantizar la detección de una amplia gama de pirógenos.
Controles positivos de pirógenos no endotoxínicos
El capítulo 2.6.30 (Prueba de activación de monocitos) de la Farmacopea Europea exige que las pruebas preparatorias incluyan al menos el receptor tipo Toll TLR4 y que se detecten al menos otros dos ligandos de receptores tipo Toll [...]. La elección de los pirógenos no endotoxinas utilizados debe reflejar los contaminantes más probables de la preparación que se examina."
Para responder a este requisito, proporcionamos una gama ampliada de controles positivos:
- Reflejan varios tipos de contaminantes que suelen encontrarse en los procesos de producción farmacéutica (bacterias Gram negativas y Gram positivas, virus y micoplasma).
- Dirigidos a varios receptores monocíticos de tipo Toll (TLR)

- Detección de un amplio espectro de pirógenos:Al igual que la prueba de pirógenos en conejo (RPT), la MAT detecta tanto endotoxinas como NEP.
- Gama ampliada de productos que pueden analizarse:
Los métodos más frecuentemente aplicados, RPT, Prueba de Endotoxinas Bacterianas (BET) y LAL, están limitados en cuanto a los tipos de productos con los que pueden utilizarse. El MAT ofrece una mayor flexibilidad en cuanto a sus aplicaciones.
- Un ensayo in vitro que imita la reacción inmunitaria humana:< Para un modelo predictivo robusto que reduzca el consumo de animales.
- Cumplimiento de las normativas y directrices internacionales:En línea con las tendencias éticas de la industria y las autoridades reguladoras para disminuir el uso de ensayos con animales.
- Sangre criopreservada extraída de 8 donantes: Para aproximarse lo más posible a la reacción inmunitaria humana a los pirógenos.
- Para reducir el consumo de animales.
Optimice o simplifique su método de prueba de pirógenos para una validación sencilla y pruebas rentables con nuestras ofertas de servicios:
- Servicios de aplicación
- Servicios de validación
- Servicios de formación
Falta de recursos para la implementación y validación de TMA. Nosotros lo haremos por usted
Estudios de viabilidad, desarrollo de métodos, validación y servicios de formación para apoyar la implementación de sus pruebas de pirógenos, hable con nuestros Pyrogen Testing Experts.
Recursos relacionados
- Brochure: PyroMAT® and PyroDetect
Used to detect a broad range of pyrogens in parenteral products such as pharmaceuticals, biopharmaceuticals or medical devices, the MAT gives an in vitro alternative to conventional animal testing in accordance with regulatory guidelines.
- Datasheet: Non-endotoxin Pyrogen Positive Controls
Meet regulatory requirements for Monocyte Activation Test (MAT) with our non-endotoxin pyrogen controls designed for the PyroMAT® system
Para seguir leyendo, inicie sesión o cree una cuenta.
¿No tiene una cuenta?