Essais sous contrat BioReliance®
Le choix du bon partenaire pour les tests analytiques et de biosécurité est essentiel dans la course à l'autorisation. Nos services de tests sous contrat BioReliance® offrent des solutions exceptionnelles qui atténuent les risques grâce à notre expertise technique et réglementaire, afin de contribuer à la mise sur le marché de médicaments qui changent la vie.
Nos services d'essai et de fabrication couvrent l'ensemble du cycle de vie du produit, du développement préclinique précoce à la production sous licence. Nos clients s'associent à nous pour répondre à leurs besoins en matière d'essais de sécurité des produits biologiques, de développement analytique et de services de biofabrication.
Une réputation qui façonne l'industrie des tests biologiques
On nous confie la sécurité des produits biologiques dans le monde entier, car pour nous, la sécurité est primordiale. Nous équilibrons les risques afin d'optimiser la vitesse de mise sur le marché sans jamais compromettre la sécurité ou la qualité. Notre force réside dans notre personnel et, avec plus de 75 ans d'expertise reconnue, nous sommes le partenaire de choix des fabricants de produits biologiques.
Parmi nos innovations les plus remarquables, citons :
1955
Élaboration de protocoles de biosécurité pour le vaccin contre la poliomyélite
1960
Développement d'un test d'anticorps sur souris en collaboration avec le NIH américain.
1983
Début des essais de biosécurité pour le premier produit à base d'anticorps monoclonaux homologué.
2007
Caractérisation des premières banques nationales américaines de cellules souches
2023
Tirer parti de la puissance du séquençage de nouvelle génération (NGS) et de notre plateforme exclusive Blazar® pour accélérer les tests et réduire l'utilisation d'animaux.
La valeur que nous apportons
Reconnus pour notre vaste portefeuille et notre expertise, nous faisons progresser le secteur grâce à nos innovations en matière d’étalons et au développement de modèles.
Flexibilité grâce à nos capacités de fabrication et d'essai – nous investissons massivement dans nos capacités et nos ressources afin de nous adapter aux besoins complexes de nos clients en matière de chaîne d'approvisionnement.
Des décennies d'expérience pour informer et guider nos clients vers l'obtention de leur autorisation. Notre expertise mondiale en matière de réglementation garantit le respect des étalons de qualité et de conformité.
Panorama de la biosécurité et de la réglementation

Développement analytique
Les approches orthogonales de caractérisation des produits permettent de mieux comprendre les performances, la sécurité et les processus de fabrication des substances médicamenteuses (DS) et des produits médicamenteux (DP).
L'identité, la pureté, la concentration et la puissance doivent être considérées collectivement afin de prendre les meilleures décisions concernant : où et comment agir, définir les spécifications et comprendre les performances.
Une partie des approches doit être intégrée au développement analytique afin de formaliser les essais et de soutenir les tests requis par les BPF pour les attributs de qualité critiques (CQA) définis par l'ICH Q6B.
Il est important de reconnaître que toutes les modalités et tous les processus sont différents, mais que les attributs qui définissent la qualité sont cohérents et doivent être compris et surveillés.
ADC
Avec les ADC, il est important de ne pas se limiter au rapport médicament/anticorps (DAR). Il est essentiel de comprendre comment les modifications post-traductionnelles et la conjugaison peuvent affecter la liaison et la puissance, car cela influe sur l'internalisation et, en fin de compte, sur la puissance.
mAbs
Dans quelle mesure comprenez-vous la relation structure-fonction de votre molécule ? Avec les mAbs, il est important de comprendre les performances de liaison, les modifications covalentes (modifications post-traductionnelles et/ou modifications involontaires) et la manière dont ces facteurs affectent les performances.
ARNm
Compte tenu des caractéristiques uniques du complexe ARNm/LNP, de nouvelles compétences et une série de capacités analytiques novatrices sont nécessaires pour garantir des vaccins et des traitements à base d'ARNm rapides, efficaces et conformes. Nous fournissons des services de test pour les matières premières ARNm, les substances médicamenteuses et les produits médicamenteux.
Thérapie cellulaire et génique
Les thérapies AAV sont complexes et présentent des défis uniques en matière de contrôle de la qualité et des performances. Ces activités nécessitent une planification et une gestion minutieuses des techniques orthogonales (par exemple, analytiques, structurelles et moléculaires). L'étendue des capacités et la coordination sont essentielles à la réussite.

Test des matières premières
L'utilisation de produits d'origine animale dans le développement ou la fabrication de produits biologiques crée un risque inhérent de contamination par des agents adventices dans les banques de cellules historiques, les virus de semence et les produits finis. Notre large gamme de services de test vise à garantir la qualité et la pureté des matières premières.

Tests sur les banques de cellules et de virus
La banque de cellules et de virus constitue le matériau de départ du processus de fabrication des produits biologiques. Une caractérisation approfondie à ce stade est importante pour garantir la sécurité virale et la stabilité génétique.
Nous mettons à profit nos décennies d'expérience dans les tests à chaque phase, de la phase préclinique à la commercialisation, afin de fournir des tests complets et des conseils réglementaires spécialisés.
Nous travaillons en partenariat avec nos clients pour réaliser une évaluation des risques afin de déterminer les facteurs susceptibles d'influencer le niveau potentiel de particules infectieuses et de caractériser efficacement la lignée cellulaire.

Tests de clairance virale
Nos études de clairance virale sont conçues par des experts en matière d'exigences réglementaires mondiales, de traitement en aval et de virologie. Ayant réalisé plus de 17 300 études de clairance virale dans nos installations aux États-Unis, au Royaume-Uni et à Singapour, les fabricants de produits biologiques nous font confiance pour minimiser les risques lors de la mise sur le marché de leurs produits.
Service de clairance Provise
Notre service Provise® Clearance déploie une équipe de scientifiques et de directeurs d'études hautement qualifiés et expérimentés qui, au nom de nos clients, effectuent toutes les étapes nécessaires du processus dans nos installations de pointe. Nous fournissons des mises à jour à chaque étape sans que les clients aient à quitter leur lieu de travail, ce qui maximise la productivité de leur équipe. Nos clients reçoivent un rapport final audité par le service de QC afin de les aider de manière experte dans leurs démarches réglementaires.
Services de validation étalons et hybrides
La réservation d'un créneau dans l'une de nos installations pour réaliser une étude de clearance virale offre une combinaison optimale de flexibilité, de productivité et d'assurance qualité. Dans un environnement convivial doté des dernières technologies, d'une grande transparence et d'un choix de forfaits de clearance étalons ou hybrides, notre équipe fournit exactement le niveau de soutien nécessaire pour les demandes IND ou BLA.

Détection virale rapide
Nous avons toujours été à l'avant-garde du secteur des tests de biosécurité grâce à nos nouvelles technologies et nos nouveaux paradigmes. Notre équipe d'experts scientifiques, réglementaires et en assurance QC dirige le développement et la sélection de méthodes de détection virale rapide afin d'accélérer les tests de biosécurité.
La plateforme Blazar® - Détection moléculaire ciblée
Notre plateforme Blazar®, première de sa catégorie, est une technologie moléculaire ciblée qui combine le multiplexage avancé et la PCR dégénérée pour détecter rapidement les virus adventices provenant de plusieurs familles virales. La plateforme Blazar® offre à nos clients une détection virale précise et hautement sensible en quelques jours seulement. Grâce à cette technologie innovante, plusieurs cibles situées dans une région conservée du génome d'une famille virale peuvent être amplifiées, ce qui permet une détection plus large par rapport aux méthodes PCR traditionnelles.
Séquençage de nouvelle génération
Révolutionnant le développement et l'analyse des thérapies biologiques, le séquençage de nouvelle génération (NGS) permet à nos clients de relever le défi de caractériser rapidement leurs produits, tout en identifiant les agents connus et inconnus. Notre gamme de services NGS conformes aux BPF repose sur des plateformes technologiques complémentaires qui génèrent rapidement des ensembles de données de séquençage approfondi pour une analyse complète des données. Elle s'appuie sur nos experts en bio-informatique et en réglementation qui fournissent des résultats rapides et complets adaptés aux besoins uniques de nos clients en matière de caractérisation des échantillons et de tests de biosécurité.

Tests de libération pour les récoltes en vrac
Qu'il s'agisse de préparer une clinique ou de fabriquer un produit biologique thérapeutique vital, il est essentiel que nos clients protègent leur investissement grâce à des tests de libération conformes aux BPF.
Nous proposons des tests conformes aux BPF pour les récoltes en vrac non transformées et purifiées afin de répondre aux exigences de leurs produits biologiques pour les études précliniques et cliniques, ainsi que pour les produits biologiques sous licence.
mAbs
Les cellules, les milieux usagés, les produits biologiques et tous les sous-produits de la réaction doivent faire l'objet de tests rigoureux afin de confirmer l'absence de tout agent adventice et de garantir leur aptitude au traitement en aval. Si la contamination n'est pas identifiée ou si les résultats inattendus ne sont pas étudiés à ce stade précoce du processus de biofabrication, cela peut entraîner une défaillance catastrophique en aval.
Thérapie cellulaire et génique
Afin de libérer le potentiel des thérapies géniques et des thérapies cellulaires génétiquement modifiées, nos services de test jouent souvent un rôle essentiel en aidant les biofabricants à garantir l'identité, la puissance et/ou la sécurité des matières premières non purifiées, des banques de cellules, des banques de virus et des plasmides utilisés dans la production de leurs produits finaux. Nous offrons une assistance conforme aux étalons cGMP pour les thérapies cellulaires et géniques, y compris celles qui utilisent l'AAV, les rétrovirus/lentivirus et les adénovirus.

Tests de libération des produits pharmaceutiques
Afin d'aider nos clients à démontrer leur conformité aux directives réglementaires avant la mise sur le marché mondial de leurs produits biologiques, nous proposons une large gamme de tests et de services d'analyse GMP pour les emballages des produits finis.
mAbs
Chaque lot d'anticorps monoclonaux produit pour des études précliniques et cliniques doit faire l'objet d'une série de tests afin de garantir que les ingrédients actifs sont exempts de contaminants, conformément aux étalons 21 CFR 211.165 et 21 CFR 610. Notre gamme complète de services de test des produits finis conformes aux BPF garantit la sécurité des patients et la conformité réglementaire dans toutes les régions du monde, avec une offre de services sur trois continents et des installations de secours pour assurer la continuité de l'approvisionnement.
Thérapie cellulaire et génique
Notre équipe d'experts consulte nos clients afin de développer un programme de tests spécifique, en s'appuyant sur une gamme de tests disponibles pour la mise sur le marché du produit final. Nous pouvons vous aider à répondre aux exigences logistiques, réglementaires et techniques uniques des thérapies avancées grâce à des méthodes de test de biosécurité et de caractérisation.
Assistance à toutes les étapes du développement de médicaments biopharmaceutiques
À chaque étape du processus de développement biopharmaceutique, nos services de biosécurité conformes aux BPF et notre expertise réglementaire peuvent aider les fabricants de produits biologiques à faire progresser leurs traitements, de la découverte à la commercialisation.
*Tests microbiologiques et autres méthodes de détection d'agents
adventices **Assistance pour les études permettant l'obtention d'une IND et d'une BLA
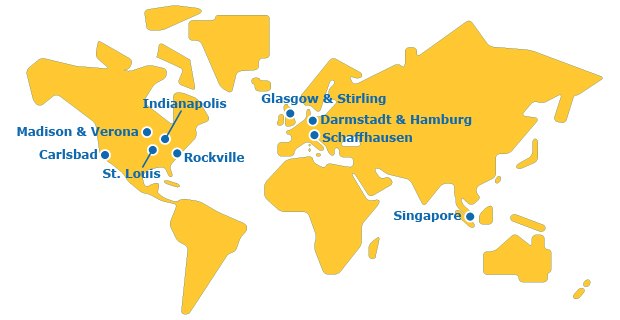
Une présence mondiale
Nous sommes une organisation unique disposant d'un réseau mondial qui fournit des services de test à toutes les étapes de la chaîne de valeur moléculaire.
Notre réseau de tests à la pointe de la technologie comprend quatre sites principaux situés à proximité des pôles biopharmaceutiques mondiaux. Les investissements continus visant à accroître la capacité de tous nos sites nous aideront à répondre à la demande croissante en matière d'études de tests de biosécurité rigoureux pour les thérapies traditionnelles et innovantes.

Notre site de services d'essais de biosécurité abrite notre banque de cellules, notre biobanque, notre service de caractérisation des lignées cellulaires et nos services d'essais de libération des substances médicamenteuses et des produits pharmaceutiques.

Notre site dispose de salles dédiées aux études de clairance virale. Notre service Provise™ Clearance Service met à votre disposition une équipe de scientifiques et de directeurs d'études hautement qualifiés et expérimentés, qui se chargent de réaliser toutes les étapes nécessaires dans notre installation ultramoderne de Stirling.

Notre site dédié aux services d'essais de biosécurité réalise la caractérisation des lignées cellulaires, la clairance virale et les essais de libération des substances médicamenteuses et des produits pharmaceutiques.

Les services de tests de biosécurité et de fabrication couvrent l'ensemble du cycle de vie du produit, depuis le développement préclinique précoce jusqu'à la production sous licence. Les services comprennent le développement analytique, la conservation de cellules, la caractérisation des lignées cellulaires, la clairance virale, les tests de libération des substances médicamenteuses et des produits pharmaceutiques, ainsi que des méthodes rapides.
Vidéo connexe
Découvrez le portail client Synetra™ nouvelle génération, conçu pour évoluer avec vos besoins. Bénéficiez d'une collaboration améliorée, de partenariats complets et de services intégrés.
Pour continuer à lire, veuillez vous connecter à votre compte ou en créer un.
Vous n'avez pas de compte ?