Sample Purification
Various chemical and physical purification methods can be applied to separate or concentrate a target analyte prior to analysis. Among these are absorption, adsorption, chromatography, distillation, extraction, ion exchange, filtration, complex formation, crystallization, drying, and many more. Sample preparation prior to analysis helps bring a sample to a format that is compatible with the analytical technique, reduces sample complexity, removes interfering impurities, and concentrates the analyte prior to analysis. Appropriate sample preparation will prevent clogging, may reduce the need for stringent washing procedures, and can extend the life of the chromatographic medium.
Featured Categories
Centrifugal and pressurized ultrafiltration devices for protein concentration, desalting, buffer exchange, separation, and diafiltration of biological and environmental samples in preparation for downstream applications.
Milli-Q® systems offer innovative water purification technologies engineered to...
Dialyzers, centrifugal ultrafiltration devices, and stirred cells for buffer exchange...
Discover our range of solid-phase extraction products for rapid and accurate analytical...
Some of the following most common purification techniques are used in the laboratory to prepare samples for downstream analysis.
Dialysis
Dialysis is a purification technique used to remove salt or other low molecular weight molecules from a sample. It is also used to exchange a sample’s buffer composition. Dialysis is a passive technique requiring large volumes of buffer.
Buffer Exchange & Desalting
Desalting is a simple method to remove salts and other low molecular weight contaminants from a sample. It is also used for buffer exchange before or after different chromatographic steps and for the rapid removal of reagents to terminate a reaction.
Fractional Precipitation
Fractional precipitation is used to remove gross impurities from small sample volumes. Precipitation techniques separate fractions by the principle of differential solubility. Because protein species differ in their degree of hydrophobicity, increased salt concentrations can enhance hydrophobic interactions between the proteins and cause precipitation.
Extraction
Sample preparation by extraction involves the isolation of target analytes from a complex sample, or much larger sample volume. The process removes interfering sample components that may block HPLC and GC columns. It also increases analyte concentration by a factor of 100 to 5,000, thereby significantly improving detection sensitivity. As part of selective and specific sample preparation, extraction helps ensure more reliable chromatographic analysis. Types of extraction are liquid-liquid extraction, solid phase extraction (SPE), and solid phase microextraction (SPME).
Affinity Chromatography
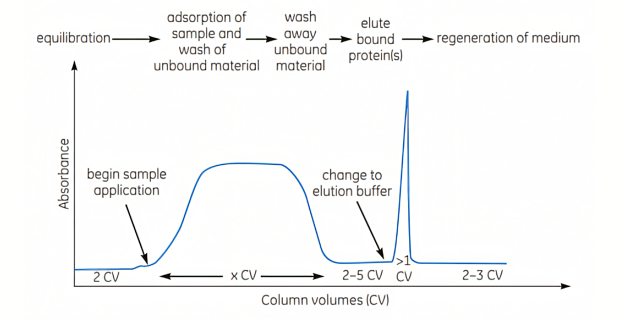
Affinity chromatography separates proteins based on reversible interactions between a protein and a specific ligand that has been coupled to a chromatography matrix. The technique is highly selective and allows for high capacity protein purification. Affinity chromatography can be used whenever a suitable ligand is available for the protein of interest.
Purification by affinity chromatography involves capture and elution steps. In the capture phase, the target protein is specifically and reversibly bound to a complementary ligand that has been immobilized on a chromatography matrix. The objective is to isolate, concentrate, and stabilize the target product, conserving its potency and activity. After washing the matrix to remove unbound material, bound target protein is recovered by changing conditions to those favoring elution. Elution is performed specifically, using a competitive ligand, or nonspecifically, by changing the pH, ionic strength, or polarity. Elution allows the target protein to be collected in a purified and concentrated form.
Visit our document search for data sheets, certificates and technical documentation.
Related Articles
- Substances are said to be miscible in one another if they dissolve to form a uniform solution. Bookmark or download our miscibility table for common lab solvents.
- How to separate proteins and peptides with affinity for metal ions by immobilized metal chelate affinity chromatography.
- This page shows volatile and non-volatile buffer suggestions for anion and cation exchange chromatography.
- Ion exchange chromatography is employed by the Genopure Plasmid Midi Kit and the Genopure Plasmid Maxi Kit.
- This page describes the maintenance of media and storage conditions for multimodal chromatography using Cytiva products.
- See All (29)
Related Protocols
- This page shows how to convert between linear flow and volumetric flow rates in affinity chromatography.
- Separation using Sephadex LH-20 column for Size Exclusion Chromatography media in polysaccharide network from Cytiva.
- In this section the practical aspect of Reverse Phased Chromatography ( RPC) is discussed including media and column selection and eluent selection and preparation.
- Superose from Cytiva are Size Exclusion Chromatography media consisting of a composite base matrix of dextran and agarose. This page shows how to perform a separation with a superose column.
- The Amberlite™ XAD-4 resin used in Porozorb™ cartridges is a proven technology that is highly effective in removing various detergents from cell culture media for biopharmaceutical applications such as vaccine production.
- See All (44)
Find More Articles and Protocols
How Can We Help
In case of any questions, please submit a customer support request
or talk to our customer service team:
Email custserv@sial.com
or call +1 (800) 244-1173
Additional Support
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- Calculators & Apps
Web Toolbox - science research tools and resources for analytical chemistry, life science, chemical synthesis and materials science.
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.