무혈청 세포 배양 조건에서 인간 유도만능줄기세포의 대장 오가노이드로의 체외 분화
오가노이드는 종종 줄기세포에서 유래된 복잡한 자가 조직화된 3차원 세포 배양 모델이다.1 오가노이드는 뇌,2 장,3 위,4 대장,5 간,6 췌장,6 폐,7 신장8 및 환자 유래 종양 등 다양한 조직에서 생성되었다.9 상피성 장 오가노이드는 종종 엔테로이드(enteroids) 또는 미니 장(mini-guts)으로 불리는 상피성 장 오가노이드는 위장관의 생리적 특성을 유지하며, 대장암, 체강 질병, 염증성 장 질환 및 숙주 미생물군 상호작용 연구를 포함한 장 발달 및 질환 모델링에 유용한 세포 배양 도구로 활용되어 왔다.10 Clevers 등이 개발한 전통적 분리 기술1은 마우스 또는 확보가 어려운 인간 조직 샘플로부터의 긴 1차 조직 분리 과정에 의존한다. 유도 만능 줄기 세포 유래 오가노이드는 더 다양한 인간 기증자로부터 환자 특이적 세포 모델을 신속하게 생성할 수 있게 할 것이다. 머크는 고도로 특성화되고 분석 준비가 완료된 냉동 보존된 인간 대장 오가노이드 및 증식 배지를 제공하는 인간 iPSC 유래 대장 오가노이드 시스템을 개발했습니다. 또한, 머크의 최적화된 무혈청 배지 및 시약은 간단한 3단계 분화 과정을 통해 모든 인간 iPS 세포주에서 대장 오가노이드를 유도하는 데 사용할 수 있습니다.
오가노이드 배양 프로토콜
단계 1: 인간 iPS 세포의 확정 내배엽 분화 (0-4일차)
참고: 약 70-80% 접합 상태이며 분화 세포가 5% 미만인 고품질 미분화 인간 ES/iPS 세포(SCC271)로 시작하십시오. 다음 프로토콜은 6웰 조직 배양 처리 플레이트의 한 웰 분화를 위한 것입니다. 표시된 용량은 단일 웰 기준입니다. 필요에 따라 용량을 조정하십시오.
- 단일 세포 배양용 배지를 준비합니다. ROCK 억제제(ROCKi) Y-27632(SCM075)를 인간 ES/iPS 확장 배지(SCM130) 7-10mL에 최종 농도 10µM이 되도록 첨가합니다.
- 6-웰 플레이트에 ECM 젤(CC131-5ML)을 코팅합니다.
- 배지를 흡입 제거합니다. DMEM/F12 또는 1X PBS 2mL로 웰을 세척합니다. 흡입 제거 후 Accumax™ (A7089) 1mL를 웰에 첨가합니다. 37°C에서 5-6분간 배양합니다. 세포를 분리하기 위해 플레이트를 손바닥에 단단히 두드립니다.
- 단일 세포 배양액(1단계에서 준비) 1mL를 웰에 첨가합니다. 5mL 피펫으로 1-3회 위아래로 피펫팅하여 세포를 분리합니다. 기포가 발생하지 않도록 주의하십시오.
- 분리된 세포를 15mL 원추형 튜브에 수집합니다. 웰에 단일 세포 배양 배지 1mL를 추가하고 잔여 세포를 모두 수집하여 세포 현탁액이 담긴 15mL 원추형 튜브로 옮깁니다. 튜브를 140 x g에서 5분간 원심분리하고 상층액을 제거합니다.
- 세포 침전물을 1mL의 단일 세포 배양액에 재현탁합니다. 트리판 블루(T8154)와 혈구계수판을 사용하여 총 생존 세포 수를 계수합니다.
- ECM 젤(CC131-5ML)로 코팅된 6-웰 플레이트의 각 웰에 1x10⁶ 세포를 첨가합니다. 사용 배지는 단일 세포 배양 배지(1단계에서 사용한 것)여야 하며, 총 용량은 웰당 3mL입니다. 37°C에서 하룻밤 동안 배양합니다.
- 웰에서 배지를 흡인 제거합니다. 웰에 최종 내배엽 유도 배지(SCM302) 2mL를 첨가하고 37°C에서 하룻밤 동안 배양합니다.
- 2일차와 3일차에도 8단계를 반복합니다. 4일차에 유세포 분석기로 세포를 분석합니다. 2단계로 진행하기 전에, 세포는 내배엽 마커 CXCR4, c-Kit, Sox-17, FOXA2에 대해 85% 이상 양성 반응을 보이고 PDGFR에 대해서는 음성 반응을 보여야 합니다.
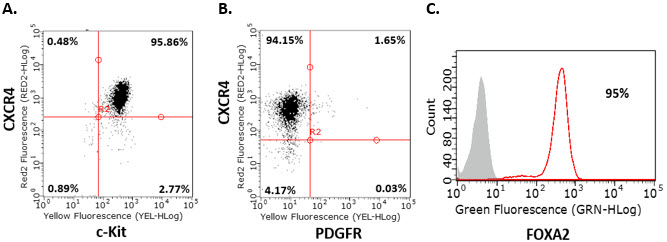
그림 2.인간 iPS 세포의 내배엽 분화. 인간 iPSC 유래 확정 내배엽 세포의 내배엽 표지자 유전자 발현을 유세포 분석한 결과, 4일간의 분화 후 세포들은 CXCR4+, c-Kit+, Sox-17+, PDGFR-, FOXA2+ 특성을 나타냄.
2단계: 후장 내배엽 분화 (4~8일차)
- 4일차 확정 내배엽 배양물이 담긴 6-웰 플레이트를 인큐베이터에서 꺼냅니다.
- 각 웰에서 배지를 흡입 제거합니다.
- 각 웰을 3mL의 1X PBS로 세척합니다.
- 각 웰에 예열된 후장 유도 배지(SCM303) 2mL를 첨가합니다.
- 플레이트를 즉시 37°C, 5% CO₂ 인큐베이터로 옮겨 24시간 동안 배양합니다.
- 2~5단계를 총 5일간 반복합니다.
- 후장 내배엽 분화 5일차는 CDX2 발현을 확인하는 중요한 시점입니다. CDX2 발현이 60% 이상이어야 단계 3으로 진행할 수 있습니다. CDX2 발현이 60% 미만일 경우, 후장 분화를 하루 더 진행한 후 CDX2 발현을 재확인하십시오.
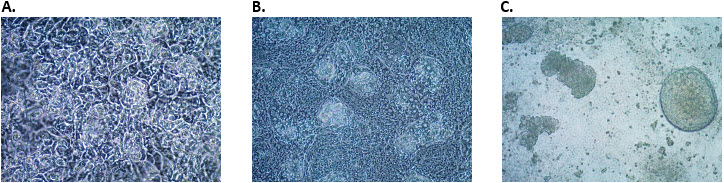
그림 3.후장 내배엽 세포로의 최종 내배엽 세포 분화. 후장 내배엽 유도 후 A) 2일차, B) 3일차 및 C) 4일차 후장 내배엽 세포의 형태.
3단계: 대장 오가노이드의 확장 및 냉동 보존 (8-48일차)
대장 오가노이드 증식
- 8일차 후장 내배엽 배양물이 담긴 6-웰 플레이트를 인큐베이터에서 꺼냅니다.
- 각 웰에서 배지를 흡인합니다.
- 각 웰을 1X PBS 3mL로 세척합니다.
- 예열된 3dGRO™ 인간 대장 오가노이드 증식 배지(SCM304) 2mL를 각 웰에 첨가합니다.
- 플레이트를 즉시 37°C, 5% CO2 인큐베이터로 옮겨 48시간 동안 배양합니다.
- 분화 12일차까지 2일마다 3dGRO™ 인간 대장 오가노이드 확장 배지(SCM304)로 배지를 교체합니다.
참고: 12일차 말에 대장 구형체가 형성되며, 3dGRO™ 인간 대장 오가노이드 확장 배지(SCM304)를 사용하여 Matrigel® 매트릭스에 매립하여 성숙한 대장 오가노이드를 생성합니다.
- Human Colon Organoid Expansion Media (SCM304)에 최종 농도 10 µM의 ROCKi Y-27632 (SCM075)를 첨가합니다.
- 성장 인자 감소 매트릭젤을 4°C에서 하룻밤 또는 얼음 위에서 충분한 양을 해동합니다.
- 대장 상피 세포 분화 12일째에 인큐베이터에서 세포를 제거하고 배지에 떠 있는 스페로이드를 15mL 원추형 튜브에 모읍니다.
- 각 웰을 3mL의 1X PBS로 세척합니다.
- 스페로이드가 포함된 단층 배양(부유하지 않는 스페로이드)을 1mL의 Accumax(A7089)로 분리하고 37°C에서 5-10분간 배양합니다.
- 단층이 느슨해지면 P-1000 피펫으로 세포를 4~5회 부드럽게 피펫팅하고, 1mL의 세포 현탁액을 위의 9단계에서 준비한 원추형 튜브로 옮깁니다.
- 4°C에서 265 x g로 5분간 원심 분리합니다.
- 상층액을 흡입하고 1X PBS 4mL로 한 번 세척합니다.
- 265 x g, 4 °C에서 5분간 원심 분리한 후 상층액을 제거합니다.
- 원추형 튜브 바닥을 가볍게 두드려 침전물을 분리합니다.
- 매트리지® 매트릭스를 TC 후드에 넣고 신속하게 1mL를 취해 16단계에서 분리된 세포 펠릿에 첨가합니다.
- 900 µL로 설정된 P-1000 피펫을 사용하여 Matrigel® 매트릭스에서 세포 펠릿을 부드럽게 재현탁시킵니다. 재현탁 과정에서 기포가 발생하지 않도록 주의하십시오.
- 겔화를 방지하기 위해 즉시 세포 현탁액을 얼음 위에 5분간 두십시오.
- 1mL의 Matrigel® 매트릭스/세포 현탁액을 신선한 Matrigel® 매트릭스로 1:50~1:100의 비율로 희석하고, 24-웰 플레이트의 각 웰에 50µL/돔을 시드합니다(예: 1:100 희석의 경우, 18단계에서 얻은 매트릭스/세포 10µL에 신선한 매트릭스 40µL를 혼합합니다. 50µL/웰을 접시에 배양합니다). 아래 그림 4를 참조하십시오.
- 24-웰 플레이트를 즉시 37 °C에서 10분간 배양합니다.
- 돔이 젤화되면 1mL의 3dGRO™ 인간 결장 오가노이드 확장 배지(SCM304) + 10µM ROCKi(SCM075)를 첨가합니다.
- 배지는 2일마다 신선한 3dGRO™ 인간 대장 오가노이드 확장 배지(SCM304) 1mL로 교체할 수 있습니다.
- 3dGRO™ 오가노이드 분해 시약(SCM300)을 사용하여 1:3에서 1:4의 분할 비율로 10-12일마다 오가노이드를 분화시킬 수 있습니다.

그림 4.인간 대장 오가노이드. A) 해동 2일 후, Matrigel® 매트릭스 돔에 캡슐화된 대장 오가노이드. B) 배양 10-12일차에 대장 오가노이드는 돔의 85-90%를 차지하며, 패시징 준비가 완료됨.
대장 오가노이드의 냉동 보존
인간 대장 오가노이드는 3dGRO™ 오가노이드 동결 배지(SCM301)를 사용하여 냉동 보존할 수 있습니다. 본 프로토콜은 냉동 보존을 위한 인간 대장 오가노이드 배양 시 분해 시약을 전혀 사용하지 않는 방식을 기반으로 합니다. 각 바이알당 권장 시작 돔 수는 4개이며, 각 돔의 밀도가 90%라고 가정합니다. 밀도가 90% 미만인 경우 바이알당 더 많은 돔을 냉동 보존하십시오.
- 오가노이드를 냉동 보존을 위해 패시징할 준비가 되면 인큐베이터에서 플레이트를 꺼냅니다.
- P-1000 피펫을 사용하여 각 Matrigel 매트릭스 돔을 기존 1mL 배지 내에서 5회 위아래로 피펫팅하여 재현탁합니다.
- 오가노이드 현탁액을 원추형 튜브로 옮깁니다.
- 10mL 피펫을 사용하여 원추형 튜브 벽을 따라 10회 피펫팅하여 오가노이드를 계속 분산시킵니다.
- 원추형 튜브를 265 x g ~ 700 x g로 원심 분리합니다.
- 상층액을 흡입하고 1X PBS 1mL로 펠릿을 재현탁시킵니다.
- P-1000 피펫을 사용하여 오가노이드 펠릿을 위아래로 20회 피펫팅하여 계속 분산시킵니다.
- 오가노이드 현탁액에 1X PBS 5mL를 첨가하고 4°C에서 700 x g로 5분간 원심 분리합니다. 상층액에 잔여 오가노이드 조각이 남아 있는 경우 추가로 5분간 원심 분리합니다.
- 상층액을 흡입하고 1mL의 3dGRO™ 오가노이드 동결 배지(SCM301)로 펠릿을 재부유시킵니다.
- P-1000 피펫으로 펠릿을 5회 재현탁한 후, 바이알당 4개의 돔에 필요한 나머지 냉동 배지 1mL를 첨가합니다.
- 냉동 보존 바이알의 세포를 냉동 용기(예: Mr. Frosty)로 옮긴 후 -80°C 냉동고에 24~72시간 동안 보관합니다.
- 냉동 보존된 인간 대장 오가노이드를 액체 질소 탱크로 옮겨 장기 보관합니다.
결과

그림 5.인간 iPS 세포 유래 대장 오가노이드의 형태학. 성숙한 인간 대장 오가노이드는 3차원 배양 시 복잡한 형태를 보인다. A) 4배 확대 B) 10배 확대
CDX2
CA-IV/DAPI
뮤신-5B/DAPI
뮤신-2/F-액틴/DAPI
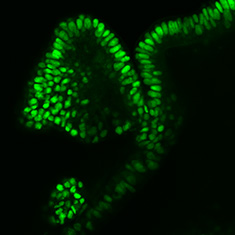
CDX2
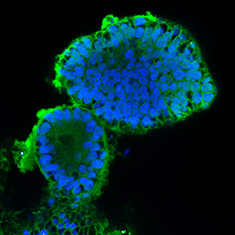
CA-II/DAPI
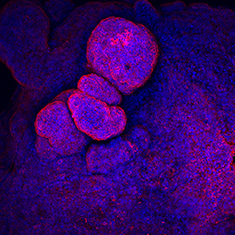
CA-IV/DAPI
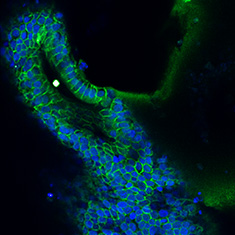
뮤신-5B/DAPI
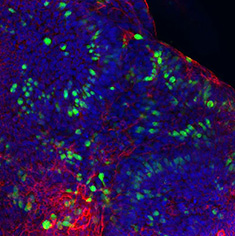
뮤신-2/F-액틴/DAPI
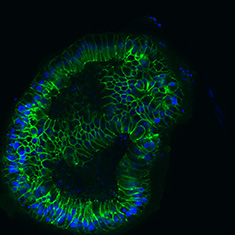
E-Cad/DAPI
그림 6. 인간 대장 오가노이드의 면역세포화학(ICC) 특성 분석. 인간 iPS 세포 유래 대장 오가노이드는 CDX2, α-탄산탈수효소-II, α-탄산탈수효소-IV, 뮤신-5B, 뮤신-2 및 E-카데린에 대해 양성 반응을 보인다.

그림 7.인간 대장 오가노이드의 면역조직화학(IHC) 특성 분석. A) 알시안 블루 염색으로 확인된 잔세포 B) Ki67 항체(적색)를 이용한 증식 세포 확인 C) H&E 염색을 이용한 핵 및 혈장 단백질 확인.
결론
머크는 인간 유도 만능 줄기 세포(iPSCs)로부터 인간 대장 오가노이드를 생성하기 위한 견고한 3단계 분화 프로토콜을 개발하였다. 이 프로토콜을 사용하여 생성된 대장 오가노이드는 성숙한 대장 표지자인 CDX2, α-탄산 탈수 효소-II, α-탄산 탈수 효소-IV, 뮤신 5B, 뮤신 2 및 E-카데린을 발현하며, 대장 표현형을 잃지 않고 여러 번의 연속적인 배양을 견딜 수 있습니다. 이러한 오가노이드와 무혈청 배지는 연구자와 신약 개발자에게 장 질환 연구를 위한 검증된 새로운 3차원 세포 모델을 제공할 것입니다.
