BioReliance®受託試験サービス
承認取得に向けた競争において、分析試験およびバイオセーフティ試験の適切なパートナー選びは極めて重要です。当社のBioReliance®受託試験サービスは、技術的および規制面での専門知識を活かし、リスクを低減する卓越したソリューションを提供することで、人々の生活を変える医薬品の市場投入を支援します。
当社の試験および製造サービスは、初期の非臨床開発から認可取得後の生産に至るまでの製品ライフサイクル全体を網羅しています。お客様は、生物製剤の安全性試験、分析開発、バイオ製造サービスに関するニーズを満たすため、当社と提携しています。
バイオ試験業界を牽引する実績
世界中の生物製剤の安全性が当社に託されているのは、私たちにとって安全がすべてだからです。安全性や品質を決して妥協することなく、リスクのバランスを取りながら市場投入までのスピードを最適化します。当社の強みは人材にあり、75年以上にわたる信頼された専門知識を活かし、バイオ製造業者にとって最適なパートナーとなっています。
当社の最も誇れるイノベーションには、以下が含まれます:
1955年
ポリオワクチンの生物安全プロトコルを策定した
1960
米国国立衛生研究所(NIH)と共同でマウス抗体検査法を開発した
1983年
初の認可を受けたモノクローナル抗体製品について、バイオセーフティ試験を開始した
2007年
米国初の全国的な幹細胞バンクを整備した
2023
次世代シーケンシング(NGS)の技術と当社独自のBlazar®プラットフォームを活用し、検査の迅速化と動物の使用削減を推進します
私たちが提供する価値
幅広いサービスラインナップと専門知識で定評があり、業界を牽引する画期的なイノベーションやテンプレートの開発に取り組んでいます。
製造・試験体制による柔軟性 – お客様の複雑なサプライチェーンのニーズに合わせて対応できるよう、当社の能力と体制に多額の投資を行っています。
数十年にわたる経験をもとに、お客様の承認取得に向けた道筋を的確に示し、導きます。当社のグローバルな規制に関するノウハウにより、品質基準とコンプライアンスの遵守を確実にします。
バイオセーフティと規制の動向

分析開発
製品の特性評価に対する多角的なアプローチは、原薬(DS)および製剤(DP)の性能、安全性、ならびに製造プロセスに対する理解を深めるのに役立ちます。
同定、純度、含量、および効力は、総合的に考慮すべきであり、それによって以下の事項に関する最適な意思決定を行うための情報となります:どこでどのように対応すべきか、仕様の設定、および性能の理解。
これらのアプローチの一部は、ICH Q6Bで定義された重要品質特性(CQA)に対してGMP下で要求される試験を支援するため、アッセイを正式に確立する目的で分析開発へと移行すべきです。
すべてのモダリティやプロセスは異なるものの、品質を定義する属性は一貫しており、それらを理解し、監視しなければならないことを認識することが重要です。
ADC
ADC では、薬物対抗体比(DAR)だけにとどまらず、その先を見据えることが重要です。翻訳後修飾や結合が結合や効力にどのような影響を与えるかを理解することは、細胞内取り込み、ひいては効力に影響を与える重要な考慮事項です。
mAbs
ご自身の分子における構造と機能の関係について、どの程度理解されていますか?mAbにおいては、結合性能、共有結合修飾(翻訳後修飾および/または意図しない修飾)、そしてそれらの要因が性能にどのように影響するかを理解することが重要です。
mRNA
mRNA/LNP複合体の特有の特性を考慮すると、迅速かつ効果的で規制要件を満たすmRNAベースのワクチンや治療薬を実現するためには、新たな専門知識と一連の革新的な分析能力が求められます。当社は、mRNAの原料、原薬、および製剤に対する試験サービスを提供しています。
細胞・遺伝子治療
AAV療法は複雑であり、品質と性能をモニタリングする上で特有の課題を抱えています。これらの活動には、相互に補完的な手法(分析、構造、分子など)の綿密な計画と管理が必要です。幅広い能力と調整が成功の鍵となります。

原材料の試験
生物製剤の開発または製造において動物由来製品を使用する場合、保存されている細胞バンク、シードウイルス、および最終製品において、外来性病原体の混入リスクが内在します。当社の幅広い試験サービスは、原材料の品質と純度を確保することを目的としています。

細胞およびウイルスバンクの試験
細胞およびウイルスバンクは、生物製剤製造プロセスの出発材料となります。この段階での詳細な特性評価は、ウイルスの安全性と遺伝的安定性を確保するために重要です。
当社は、前臨床から商業化に至るまでの各段階における数十年にわたる試験実績を活かし、包括的な試験と専門的な規制に関するガイダンスを提供します。
当社はお客様と連携し、リスク評価を実施して、潜在的な感染性粒子レベルに影響を与える可能性のある要因を特定し、細胞株を効果的に特性評価します。

ウイルス除去試験
当社のウイルス除去試験は、世界各国の規制要件、後工程、およびウイルス学の専門家によって設計されています。米国、英国、シンガポールの各施設で17,300件以上のウイルス除去試験を実施してきた実績があり、バイオ医薬品メーカー各社は、自社製品を市場に投入する際のリスクを最小限に抑えるため、当社を信頼していただいています。
Provise® クリアランス・サービス
当社のProvise®クリアランスサービスでは、高度な訓練を受け、豊富な経験を持つプロセスサイエンティストおよびスタディディレクターのチームを派遣し、最先端の施設において必要なすべてのプロセスステップを代行して実施します。お客様が職場を離れることなく、各ステップの進捗状況を随時ご報告することで、チームの生産性を最大化します。お客様には、規制当局への申請を専門的にサポートする、品質保証(QA)監査済みの最終報告書をお渡しします。
スタンダードおよびハイブリッド・クリアランス・サービス
当社の施設でウイルス除去試験を実施するための時間を予約することで、柔軟性、生産性、品質保証の最適な組み合わせを実現できます。最新技術、透明性、そしてスタンダードまたはハイブリッドの除去パッケージの選択を特徴とする使いやすい環境において、当社のチームは、INDまたはBLA申請に向けた取り組みにおいて、まさに必要なレベルのサポートを提供します。

ウイルスの迅速検出
当社は、新たな技術とパラダイムを通じて、バイオセーフティ試験業界を牽引してきた実績があります。科学、規制、品質保証の専門家からなる当社のチームは、バイオセーフティ試験の迅速化を図るため、迅速なウイルス検出法の開発と選定を主導しています。
Blazar®プラットフォーム - 標的分子検出
業界初のBlazar®プラットフォームは、高度なマルチプレックス技術とデジェネレートPCRを組み合わせたターゲット型分子技術であり、複数のウイルス科に属する外来ウイルスを迅速に検出します。Blazar®プラットフォームは、わずか数日で正確かつ高感度のウイルス検出をクライアントに提供します。この革新的な技術を活用することで、ウイルス科ゲノムの保存領域内にある複数のターゲットを増幅することができ、従来のPCR法と比較してより広範な検出範囲を実現します。
次世代シーケンシング
生物学的製剤の開発と解析に革命をもたらす次世代シーケンシング(NGS)により、お客様は既知および未知の病原体を特定しつつ、自社製品の迅速な特性評価という課題に対応することが可能になります。 当社のGMP準拠NGSサービス群は、包括的なデータ解析のためのディープシーケンスデータセットを迅速に生成する相互補完的な技術プラットフォームに基づいています。これに加え、バイオインフォマティクスおよび規制の専門家が、お客様の独自のサンプル特性評価やバイオセーフティ試験のニーズに合わせた迅速かつ包括的な結果を提供します。

大量収穫後の出荷検査
臨床試験の準備であれ、人命を救う治療用生物製剤の製造であれ、お客様がGMP準拠の出荷検査を通じて投資を保護することは極めて重要です。
当社は、前臨床試験および臨床試験用の生物学的製剤、ならびに承認済み生物学的製剤の要件を満たすため、未処理および精製済みのバルクハーベストに対するGMP準拠の試験を提供しています。
モノクローナル抗体(mAbs)
細胞、使用済み培地、生物学的製剤、および反応の副産物については、外来性微生物の混入がないことを確認し、下流工程への適性を保証するために、厳格な試験が必要です。バイオ製造プロセスのこの初期段階で汚染を特定できなかったり、予期せぬ結果を調査しなかったりすると、下流工程で壊滅的な失敗につながる可能性があります。
細胞・遺伝子治療
遺伝子治療および遺伝子改変細胞治療の可能性を最大限に引き出すため、当社の試験サービスは、バイオ製造業者が最終製品の製造に使用する未精製バルク、原材料、細胞バンク、ウイルスバンク、およびプラスミドの同一性、効力、および/または安全性を確保する上で、しばしば重要な役割を果たしています。 当社は、AAV、レトロウイルス/レンチウイルス、アデノウイルスなどを利用するものを含め、細胞・遺伝子治療に対してcGMP準拠のサポートを提供しています。

医薬品出荷前検査
お客様がバイオ医薬品を世界の医薬品市場に発売する前に、規制ガイドラインへの準拠を実証できるよう、当社は最終製品パッケージ向けの幅広いGMP試験および検査サービスを提供しています。
モノクローナル抗体
前臨床および臨床試験用に製造されるモノクローナル抗体の各ロットは、21 CFR 211.165および21 CFR 610に基づき、有効成分に不純物が含まれていないことを確認するための一連の試験が必要です。当社の包括的なGMP準拠の最終製品試験サービスは、3大陸でのサービス提供と供給継続性を確保するためのバックアップ施設を備え、あらゆる地域において患者の安全性と規制順守を保証します。
細胞・遺伝子治療
当社の専門家チームは、お客様と協議の上、最終製品のリリースに向けた多様なプラットフォームアッセイを活用し、特定の試験プログラムを策定します。当社は、バイオセーフティおよび特性評価試験手法を用いて、先進医療特有の物流、規制、技術的要件への対応を支援します。
バイオ医薬品開発の全段階におけるサポート
バイオ医薬品開発プロセスのどの段階においても、当社の最先端のGMP準拠バイオセーフティサービスと規制に関する知見は、バイオ医薬品メーカーが創薬から上市に至るまでのプロセスを推進する上で役立ちます。
*微生物学的検査およびその他の外来性微生物検出法 **INDおよびBLA
申請に向けた試験の支援
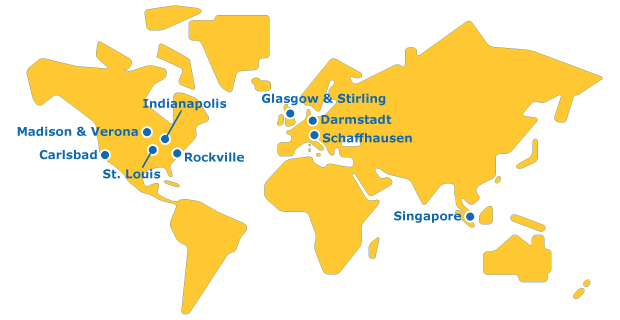
世界的な展開
当社は、分子バリューチェーンの全段階にわたる試験サービスを提供する、グローバルネットワークを有する単一組織です。
当社の最先端の試験ネットワークは、世界のバイオ医薬品拠点の近くに位置する4つの主要拠点で構成されています。全拠点における生産能力の拡大に向けた継続的な投資により、従来型および新規治療法に対する堅牢なバイオセーフティ試験への高まる需要に応えていきます。

当社のバイオセーフティ試験サービス拠点では、細胞バンクの製造、バイオレポジトリ、細胞株の特性評価、ならびに原薬および製剤のリリース試験サービスを提供しています。

当社施設には、ウイルス除去試験用の専用スイートが完備されています。当社の「Provise™ クリアランス・サービス」では、高度な訓練を受け、豊富な経験を持つプロセス科学者および試験責任者からなるチームを派遣し、最先端のスターリング施設にて、お客様が必要とするすべてのプロセス工程を実施いたします。

当社のバイオセーフティ試験サービス部門では、細胞株の特性評価、ウイルス除去試験、および原薬・製剤の出荷試験を実施しています。

バイオセーフティ試験および製造サービスは、初期の非臨床開発から認可生産に至るまでの製品ライフサイクル全体を網羅しています。サービス内容には、分析法の開発、細胞バンク、細胞株の特性評価、ウイルス除去、原薬および製剤のリリース試験、ならびに迅速分析法が含まれます。
関連動画
お客様のニーズに合わせて進化する、次世代クライアントポータル「Synetra™」をご覧ください。強化されたコラボレーション機能、包括的なパートナーシップ、そして統合されたサービスをご体験ください。
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?